题目内容
已知:t℃下的某一气态平衡体系中含有 X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为:K=
,有关该平衡的说法中正确的是( )
| c(X)?c2(Y) |
| c2(Z)?c2(W) |
| A、升高温度,平衡常数K变大 |
| B、增大压强,W(g)的物质的量分数变大 |
| C、升温,若混合气体的相对分子质量变小,则逆反应放热 |
| D、增大Z浓度,平衡向正反应方向移动 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:已知:t℃下的某一气态平衡体系中含有 X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为:K=
,则化学方程式为:
2Z(g)+2W(g)?X(g)+2Y(g),反应是气体体积减小的反应,反应热量变化不知,依据化学平衡移动原理分析判断.
| c(X)?c2(Y) |
| c2(Z)?c2(W) |
2Z(g)+2W(g)?X(g)+2Y(g),反应是气体体积减小的反应,反应热量变化不知,依据化学平衡移动原理分析判断.
解答:
解:已知:t℃下的某一气态平衡体系中含有 X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为:K=
,则化学方程式为:2Z(g)+2W(g)?X(g)+2Y(g),反应是气体体积减小的反应,反应热量变化不知;
A、升温平衡向吸热反应方向进行,但反应热量变化不知,不能判断平衡常数变化,故A错误;
B、增大压强平衡向气体体积减小的分析进行,平衡正向进行,W质量分数减小,故B错误;
C、升温,若混合气体的相对分子质量变小,说明气体物质的量增大,则逆反应吸热反应,故C错误;
D、增大Z浓度,增大反应物浓度,平衡向正反应方向移动,故D正确;
故选D.
| c(X)?c2(Y) |
| c2(Z)?c2(W) |
A、升温平衡向吸热反应方向进行,但反应热量变化不知,不能判断平衡常数变化,故A错误;
B、增大压强平衡向气体体积减小的分析进行,平衡正向进行,W质量分数减小,故B错误;
C、升温,若混合气体的相对分子质量变小,说明气体物质的量增大,则逆反应吸热反应,故C错误;
D、增大Z浓度,增大反应物浓度,平衡向正反应方向移动,故D正确;
故选D.
点评:本题考查了化学平衡影响因素分析判断,化学平衡常数和化学平衡移动原理是解题关键,题目难度中等.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列物质属于强电解质且能导电的是( )
(1)氯化钠溶液;(2)氯化铵固体;(3)铜;(4)石墨;(5)熔融NaOH;(6)稀硫酸;(7)醋酸.
(1)氯化钠溶液;(2)氯化铵固体;(3)铜;(4)石墨;(5)熔融NaOH;(6)稀硫酸;(7)醋酸.
| A、(1)(2)(5)(6) |
| B、(5) |
| C、(2)(5)(7) |
| D、(1)(3)(4)(5)(6) |
下列反应中,通过置换反应得到铁的是( )
| A、铜浸入氯化铁溶液中 |
| B、一氧化碳通过炽热的氧化铁 |
| C、铝和Fe2O3混合物加热至高温 |
| D、铜浸入氯化亚铁溶液中 |
下列对葡萄糖性质的叙述中错误的是( )
| A、葡萄糖具有醇羟基,能和酸起酯化反应 |
| B、葡萄糖能使溴水褪色 |
| C、葡萄糖能被硝酸氧化 |
| D、葡萄糖能水解生成乙醇 |
下列四种溶液中一定存在SO42-的是( )
| A、向甲溶液中加入BaCl2溶液,产生白色沉淀 |
| B、向乙溶液中加入BaCl2溶液,有白色沉淀,再加入盐酸,沉淀不溶解 |
| C、向丙溶液中加入盐酸使之酸化无现象,再加入BaCl2溶液,有白色沉淀 |
| D、向丁溶液中加入硝酸使之酸化,再加入硝酸钡溶液,有白色沉淀 |
设NA为阿伏伽德罗常数,下列有关叙述中正确的是( )
| A、标准状况下,2.24L Cl2完全溶于水,反应中转移的电子数为0.1NA |
| B、标准状况下,1.12L CCl4中含有的C-Cl键的数目大于0.2NA |
| C、某密闭容器中装有23g NO2气体,则含有的原子数小于1.5NA |
| D、58.5g的氯化钠固体中含氯化钠分子数为NA |
新弹性材料丁基苯呲橡胶的结构简式如图.

其单体可能是以下物质中的某几种正确的一组单体是( )
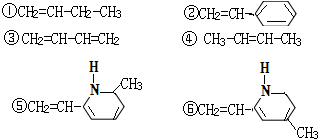

其单体可能是以下物质中的某几种正确的一组单体是( )

| A、①②⑥ | B、②③⑤ |
| C、①②⑤ | D、②④⑥ |
一定条件下的密闭容器中有如下反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905.9kJ?mol-1,下列叙述正确的是( )
| A、平衡后减小压强,混合气体平均摩尔质量增大 | ||
B、平衡时v正(O2)=
| ||
| C、4 mol NH3和5 mol O2反应,达到平衡时放出热量为905.9 kJ | ||
| D、平衡后升高温度,混合气体中NO含量降低 |