题目内容
一定条件下的密闭容器中有如下反应:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-905.9kJ?mol-1,下列叙述正确的是( )
| A、平衡后减小压强,混合气体平均摩尔质量增大 | ||
B、平衡时v正(O2)=
| ||
| C、4 mol NH3和5 mol O2反应,达到平衡时放出热量为905.9 kJ | ||
| D、平衡后升高温度,混合气体中NO含量降低 |
考点:化学平衡的影响因素,化学平衡的计算
专题:化学平衡专题
分析:A.反应为可逆反应,反应物不可能完全转化;
B.达到平衡时,正逆反应速率相等;
C.减小压强,平衡向正反应方向移动;
D.升高温度,平衡向逆反应方向移动.
B.达到平衡时,正逆反应速率相等;
C.减小压强,平衡向正反应方向移动;
D.升高温度,平衡向逆反应方向移动.
解答:
解:A.减小压强,平衡向正反应方向移动,混合气体平均摩尔质量减小,故A错误;
B.达到平衡时,正逆反应速率相等,应为v正(O2)=
v逆(NO),故B错误;
C.反应为可逆反应,反应物不可能完全转化,则4mol NH3和5mol O2反应,达到平衡时放出热量小于905.9kJ,故C错误;
D.升高温度,平衡向逆反应方向移动,混合气体中NO含量降低,故D正确.
故选:D.
B.达到平衡时,正逆反应速率相等,应为v正(O2)=
| 5 |
| 4 |
C.反应为可逆反应,反应物不可能完全转化,则4mol NH3和5mol O2反应,达到平衡时放出热量小于905.9kJ,故C错误;
D.升高温度,平衡向逆反应方向移动,混合气体中NO含量降低,故D正确.
故选:D.
点评:本题考查化学平衡的影响,题目难度中等,本题注意把握可逆反应的特点,注意外界条件对化学平衡的影响.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
已知:t℃下的某一气态平衡体系中含有 X(g)、Y(g)、Z(g)、W(g)四种物质,此温度下发生反应的平衡常数表达式为:K=
,有关该平衡的说法中正确的是( )
| c(X)?c2(Y) |
| c2(Z)?c2(W) |
| A、升高温度,平衡常数K变大 |
| B、增大压强,W(g)的物质的量分数变大 |
| C、升温,若混合气体的相对分子质量变小,则逆反应放热 |
| D、增大Z浓度,平衡向正反应方向移动 |
m g铜和足量的浓硫酸反应,生成SO2 n L,则被还原的硫酸是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列微粒的核外电子的表示方法中正确的是( )
A、基态碳原子的电子排布图 |
B、基态铜原子核外的3d、4s轨道内电子排布图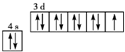 |
| C、Cl的外围电子排布式3s13p6 |
| D、Fe2+的电子排布式1s22s22p63s23p63d6 |
下列各组物质既能与强酸反应,且受热后能产生刺激性气味气体的是( )
| A、氯化铵溶液 |
| B、碳酸氢钾溶液 |
| C、碳酸氢铵溶液 |
| D、硫酸氢钠溶液 |
X、Y、Z三种元素,已知X和Y原子核外电子层数相同,Y和Z原子最外层电子数相同,又知三种元素原子最外层电子数总和为14,而质子数总和为28,则三种元素为( )
| A、N、P、O |
| B、N、C、Si |
| C、B、Mg、Al |
| D、C、N、P |
NA代表阿伏加德罗常数的值.下列叙述中正确的是( )
| A、标准状况下,2.24L CH2Cl2含有分子的数目为0.1NA |
| B、常温常压下,46g的NO2和N2O4混合气体含有的原子数为3NA |
| C、在标准状况下,11.2L NO与11.2L O2混合后气体分子数为0.75NA |
| D、1mol FeCl3完全水解得到的Fe(OH)3胶体中含有的胶粒的数目为1NA |
下列说法正确的是( )
| A、简单离子的核外电子排布一定与上一周期稀有气体元素原子的核外电子排布相同 |
| B、多电子原子中,在离核较近的区域内运动的电子能量较低 |
| C、同主族元素,从上到下离子半径依次增大;同周期元素,从左到右离子半径依次减小 |
| D、过渡元素均为金属元素,属于副族元素 |
同主族元素所形成的同一类化合物,其结构和性质往往相似,化合物PH4I是一种无色晶体,下列对它的描述中错误的是( )
| A、它是共价化合物 |
| B、在加热时,它能分解 |
| C、它能跟碱发生反应 |
| D、它可由PH3和HI化合而成 |