题目内容
1.下列说法正确的是( )| A. | 氯化铁溶液有较强氧化性,故可用作净水剂 | |
| B. | 煤中含有大量的有机物,用干馏的方法通过发生物理变化得到产物 | |
| C. | 除去CH4中的少量C2H4:通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 将ag铜丝灼烧成黑色后趁热插入乙醇中,铜丝变红,再次称量质量等于a g |
分析 A、氯化铁的净水作用是利用铁离子水解生成氢氧化铁胶体具有吸附悬浮杂质的作用;
B、煤的干馏是复杂的物理化学变化;
C、乙烯被酸性高锰酸钾溶液氧化生成二氧化碳气体;
D、氧化铜与乙醇发生氧化还原反应,铜丝灼烧成黑色,立即放入乙醇中,CuO与乙醇反应生成铜.
解答 解:A、氯化铁有氧化性,但不是做净水剂的原因,净水是利用 铁离子水解生成的氢氧化铁胶体具有吸附性,能吸附悬浮的杂质净水,故A错误;
B、煤的干馏是复杂的物理、化学变化,干馏得到产物是发生化学反应生成,故B错误;
C、乙烯被酸性高锰酸钾溶液氧化生成二氧化碳气体,甲烷气体中混入新的杂质二氧化碳,故C错误;
D、铜丝灼烧成黑色,立即放入乙醇中,CuO与乙醇反应:CuO+C2H5OH$\stackrel{△}{→}$CH3CHO+Cu+H2O,反应前后其质量不变,故D正确;
故选D.
点评 本题考查有机物的性质,物质制备方法,主要是乙烯、乙醇的性质的理解应用,掌握基础是解题关键,题目难度中等.

练习册系列答案
相关题目
6.已知C2H5OH的质量分数为10%的乙醇溶液的密度是0.982g•cm-3,则该酒精溶液中乙醇的物质的量浓度是( )
| A. | 9.82mol•L-1 | B. | 4.91mol•L-1 | C. | 2.13mol•L-1 | D. | 1.12mol•L-1 |
9.在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:下列叙述错误的是( )
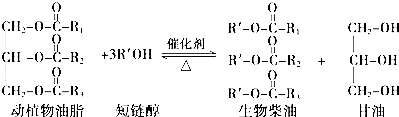
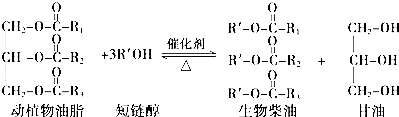
| A. | 生物柴油由可再生资源制得 | B. | 生物柴油是不同酯组成的混合物 | ||
| C. | “地沟油”可用于制备生物柴油 | D. | 动植物油脂与醇的反应是皂化反应 |
16.下列各组中,分子数目相同的是( )
| A. | 22.4 L氩气和1 mol氢气 | |
| B. | 2 g氢气和16 g氧气 | |
| C. | 同温同压下,2 L氢气和2 L水 | |
| D. | 常温常压下1 mol氧气和标准状况下2 g氢气 |
6.下表对某些反应方程式的评价合理的是( )
| 编号 | 离子方程式或电极方程式 | 评价 | |
| A | Ca(ClO)2溶液中通入足量SO2 | Ca2++ClO-+SO2+H2O=CaSO4+Cl-+2H+ | 正确 |
| B | Ba(OH)2溶液中加入过量Al2(SO4)3溶液 | 3Ba2++6OH-+2Al3++3SO42-=3BaSO4↓+2Al(OH)3↓ | 正确 |
| C | 醋酸铵溶于水 | CH3COO-+NH4+?CH3COOH+NH3•H2O | 错误,阴阳离子水解相互促进,应该用“=”号 |
| D | 用惰性电极电解 CuCl2和NaCl的混合溶液一段时间 | 阴极:Cu2++2e-=Cu 阳极:4OH--4e-=2H2O+O2 | 错误,只因为两级得失电子没配平 |
| A. | A | B. | B | C. | C | D. | D |
13.25℃时,水的电离达到平衡:H2O?H++OH-;△H>0,下列叙述正确的是( )
| A. | 向水中加入稀氨水,平衡逆向移动,[OH-]降低 | |
| B. | 向水中加入少量固体硫酸氢钠,[H+]增大,KW不变 | |
| C. | 将水加热至95℃,pH<7,说明加热可导致水呈酸性 | |
| D. | 将水加热至95℃,仍然呈中性,KW不变 |
10.实验室可用如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是( )

| A. | NO2 | B. | NO | C. | SO2 | D. | NH3 |
11.设NA为阿伏加德罗常数的值,下列有关叙述不正确的是( )
| A. | 标准状况下,1L乙烷所含有的分子数为NA/22.4 | |
| B. | 1mol甲基(-CH3)所含电子数为9NA | |
| C. | 常温下,28g C2H4含NA个碳碳双键 | |
| D. | 1L0.1mol•L-1乙酸溶液中H+数为0.1NA |