题目内容
一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。工业上依此用CO生产燃料甲醇。
CH3OH(g)。工业上依此用CO生产燃料甲醇。
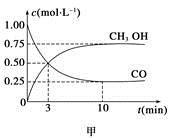
(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(CO)=__________________。
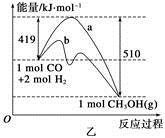
(2)乙图表示该反应进行过程中能量的变化。曲线b下的反应条件为 。该反应的焓变是________(填“ΔH<0”或“ΔH>0”),写出反应的热化学方程式 ;选择适宜的催化剂______(填“能”或“不能”)改变该反应的反应热。
(3)该反应平衡常数K的表达式为______________________,温度升高,平衡常数K________(填“增大”、“不变”或“减小”)。
(4)恒容条件下,下列措施中能使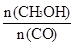 增大的有____________。
增大的有____________。
a.降低温度 b.充入He气
c.再充入1molCO和2molH2 d.使用催化剂
 CH3OH(g)。工业上依此用CO生产燃料甲醇。
CH3OH(g)。工业上依此用CO生产燃料甲醇。

(1)甲图是反应时CO和CH3OH(g)的浓度随时间变化情况。从反应开始到平衡,用H2浓度变化表示平均反应速率v(CO)=__________________。
(2)乙图表示该反应进行过程中能量的变化。曲线b下的反应条件为 。该反应的焓变是________(填“ΔH<0”或“ΔH>0”),写出反应的热化学方程式 ;选择适宜的催化剂______(填“能”或“不能”)改变该反应的反应热。
(3)该反应平衡常数K的表达式为______________________,温度升高,平衡常数K________(填“增大”、“不变”或“减小”)。
(4)恒容条件下,下列措施中能使
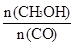 增大的有____________。
增大的有____________。a.降低温度 b.充入He气
c.再充入1molCO和2molH2 d.使用催化剂
(1)0.075 mol·L-1·min-1
(2)加催化剂,ΔH<0 ,CO(g)+2H2(g) CH3OH(g) ΔH=-91 kJ·mol-1不能
CH3OH(g) ΔH=-91 kJ·mol-1不能
(3)K=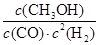 减小
减小
(4)ac
(2)加催化剂,ΔH<0 ,CO(g)+2H2(g)
 CH3OH(g) ΔH=-91 kJ·mol-1不能
CH3OH(g) ΔH=-91 kJ·mol-1不能(3)K=
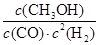 减小
减小(4)ac
(1)化学反应速率就是指单位时间内浓度的变化量。由图知,V(CO)="0.075" mol·L-1·min-1;
(2)曲线a和曲线b的明显区别是反应的活化能不一样,表明曲线b是使用了催化剂,从图中可以看出和出的热量比吸收的热量多,因此是放热反应:ΔH<0; CO(g)+2H2(g) CH3OH(g) ΔH=-91 kJ·mol-1;催化剂不能改变反应的反应热。
CH3OH(g) ΔH=-91 kJ·mol-1;催化剂不能改变反应的反应热。
(3)K=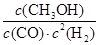 ;升高温度平衡向逆方向移动,K减少;
;升高温度平衡向逆方向移动,K减少;
(4)降低温度,平衡正向移动,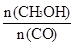 增大;充入He气,浓度不变,平衡不移动;C相当于增大压强,平衡正向移动;加入催化剂化学平衡不移动。
增大;充入He气,浓度不变,平衡不移动;C相当于增大压强,平衡正向移动;加入催化剂化学平衡不移动。
(2)曲线a和曲线b的明显区别是反应的活化能不一样,表明曲线b是使用了催化剂,从图中可以看出和出的热量比吸收的热量多,因此是放热反应:ΔH<0; CO(g)+2H2(g)
 CH3OH(g) ΔH=-91 kJ·mol-1;催化剂不能改变反应的反应热。
CH3OH(g) ΔH=-91 kJ·mol-1;催化剂不能改变反应的反应热。(3)K=
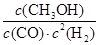 ;升高温度平衡向逆方向移动,K减少;
;升高温度平衡向逆方向移动,K减少;(4)降低温度,平衡正向移动,
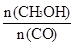 增大;充入He气,浓度不变,平衡不移动;C相当于增大压强,平衡正向移动;加入催化剂化学平衡不移动。
增大;充入He气,浓度不变,平衡不移动;C相当于增大压强,平衡正向移动;加入催化剂化学平衡不移动。
练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
 a Z(g)。
a Z(g)。 CH3OH(g)
CH3OH(g)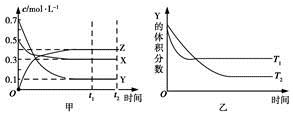
 2Z(g) ΔH>0
2Z(g) ΔH>0 CH3OH(g) +H2O(g) △H
CH3OH(g) +H2O(g) △H
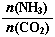 =3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为: 。
=3,达平衡时CO2的转化率为60%,则NH3的平衡转化率为: 。 CO2(g)+2H2O(g)
CO2(g)+2H2O(g)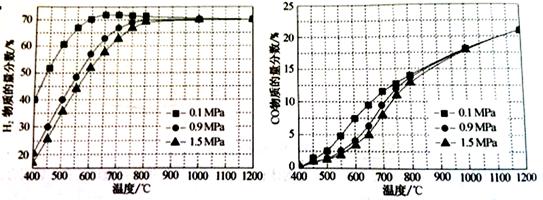
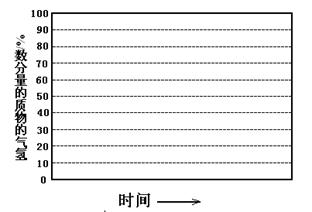
 2NH3(g)(正反应为放热反应)。下列说法错误的是
2NH3(g)(正反应为放热反应)。下列说法错误的是