题目内容
元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
| A、同一元素的单质,不可能既能与酸反应,又能与碱反应 |
| B、IA族元素的金属性一定比IIA族元素的金属性强 |
| C、第三周期元素的最高正化合价等于它所处的主族序数 |
| D、短周期中,同周期元素的离子半径从左到右逐渐减小 |
考点:元素周期表的结构及其应用
专题:元素周期律与元素周期表专题
分析:A.同一元素的单质,可能既能与酸反应,又能与碱反应;
B.IA族元素的金属性不一定比IIA族元素的金属性强,但同一周期的IA族元素的金属性一定比IIA族元素的金属性强;
C.主族元素中其最高正化合价等于其族序数(O、F除外);
D.短周期元素同一周期中,离子半径先减小后增大.
B.IA族元素的金属性不一定比IIA族元素的金属性强,但同一周期的IA族元素的金属性一定比IIA族元素的金属性强;
C.主族元素中其最高正化合价等于其族序数(O、F除外);
D.短周期元素同一周期中,离子半径先减小后增大.
解答:
解:A.同一元素的单质,可能既能与酸反应,又能与碱反应,如Al,故A错误;
B.IA族元素的金属性不一定比IIA族元素的金属性强,如Ca的金属性大于Li,故B错误;
C.主族元素中其最高正化合价等于其族序数(O、F除外),所以第三周期元素的最高正化合价等于它所处的主族序数,故C正确;
D.短周期元素同一周期中,离子的电子层数有2个电子层的和3个电子层的,电子层结构相同的离子,离子半径随着原子序数增大而减小,电子层数越多其离子半径越大,所以短周期中,同周期元素的离子半径从左到右先减小后增大,故D错误;
故选C.
B.IA族元素的金属性不一定比IIA族元素的金属性强,如Ca的金属性大于Li,故B错误;
C.主族元素中其最高正化合价等于其族序数(O、F除外),所以第三周期元素的最高正化合价等于它所处的主族序数,故C正确;
D.短周期元素同一周期中,离子的电子层数有2个电子层的和3个电子层的,电子层结构相同的离子,离子半径随着原子序数增大而减小,电子层数越多其离子半径越大,所以短周期中,同周期元素的离子半径从左到右先减小后增大,故D错误;
故选C.
点评:本题考查了原子结构和元素性质,根据物质的性质、原子结构结合元素周期律分析解答,B为易错选项,要分析不同周期元素,题目难度不大.

练习册系列答案
 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
山梨酸是一种常用的食品防腐剂,其结构简式如图所示,下列关于山梨酸的说法不正确的是( )


| A、其分子式为C7H10O5 |
| B、分子中含有三种官能团 |
| C、1mol该物质能与3mol NaOH溶液反应 |
| D、能使溴的四氯化碳溶液或酸性高猛酸钾溶液褪色 |
下列符号中“2”的含义依次正确的一组是( )
H 2He 2Cl Ca2+.
2 1 |
| A、质量数 中子数 质子数 电荷数 |
| B、质子数 中子数 原子个数 电荷数 |
| C、质量数 质子数 原子个数 电荷数 |
| D、质量数 质子数 中子数 电荷数 |
第3周期元素的基态原子中,不可能出现d电子,主要依据是( )
| A、能量守恒原理 | B、泡利原理 |
| C、洪特规则 | D、构造原理 |
下列事实没有体现出胶体的性质的是( )
| A、向煮熟的豆浆中加入石膏或卤水以生产豆腐 |
| B、工厂用高压电极除粉尘 |
| C、氢氧化铁胶体中加入足量稀硫酸形成黄色溶液 |
| D、午后林间透过缕缕阳光 |
某化学学习小组学习电化学后,设计了下面的实验装置图:
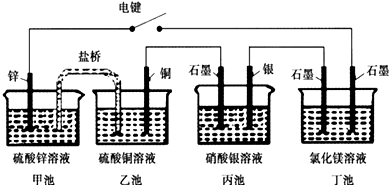
下列有关该装置图的说法中正确的是( )

下列有关该装置图的说法中正确的是( )
| A、合上电键后,盐桥中的阳离子向甲池移动 |
| B、合上电键后,丙池为电镀银的电镀池 |
| C、合上电键后一段时间,丙池中溶液的pH增大 |
| D、合上电键后一段时间,当丙池中生成标准状况下560mL气体时,丁池中理论上最多产生2.9g固体 |