题目内容
【题目】(1)有下列五种烃:

其中互为同分异构体的是_________________(填序号),②③④⑤四种物质按它们的沸点由低到高的顺序是________________(填序号),等质量的①③⑥三种物质,完全燃烧时消耗O2的物质的量由少到多的顺序为________________ 。
(2) 的系统命名为___________________;
的系统命名为___________________;
(3)分子式为C2H6O的有机物,有两种同分异构体,乙醇(CH3CH2OH)、二甲醚(CH3OCH3),则通过下列方法,不可能将二者区别开来的是 ______
A.红外光谱 B. 1H核磁共振谱 C.质谱法 D.与钠反应
(4)已知乙烯分子是平面结构, 1,2-二氯乙烯可形成![]() 和
和![]() 两种不同空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是_____
两种不同空间异构体,称为顺反异构。下列能形成类似上述空间异构体的是_____
A.1-丙烯 B.4-辛烯 C.1-丁烯 D.2-甲基-1-丙烯
【答案】 ②④ ③<⑤<②<④ ⑥<①<③ 2,2,6-三甲基-4-乙基辛烷 D B
【解析】试题分析:(1)同分异构体是分子式相同、结构不同的有机物;随碳原子数的增多,烃的沸点升高,碳原子数相同,支链越少沸点越高;等质量的烃完全燃烧,氢元素质量分数越大耗氧量越大。(2)根据有机物系统命名原则命名;(3)红外光谱能测官能团种类、核磁共振谱能测“等效氢”、质谱法测相对分子质量、与钠反应可以检验羟基;(4)顺反异构是双键碳两侧碳原子所连原子或原子团不同;
解析:(1)①分子式是C4H8,②分子式是C5H12,③分子式是C3H8,④分子式是C5H12,⑤分子式是C4H10,⑥分子式是C8H10,②④分子式相同,结构不同,属于同分异构体;随碳原子数的增多,烃的沸点升高,碳原子数相同,支链越少沸点越高,所以②③④⑤四种物质按它们的沸点由低到高的顺序是③<⑤<②<④;等质量的烃完全燃烧,氢元素质量分数越大耗氧量越大,①③⑥氢元素的含量分别是![]() 、
、![]() 、
、![]() ,所以完全燃烧时消耗O2的物质的量由少到多的顺序为⑥<①<③。(2)根据系统命名原则,主链最长、从离支链最近的一端给主链碳原子编号,
,所以完全燃烧时消耗O2的物质的量由少到多的顺序为⑥<①<③。(2)根据系统命名原则,主链最长、从离支链最近的一端给主链碳原子编号, 的名称是2,2,6-三甲基-4-乙基辛烷;(3)红外光谱能测官能团,乙醇(CH3CH2OH)、二甲醚(CH3OCH3)官能团不同,红外光谱可以鉴别;核磁共振谱能测“等效氢”,乙醇(CH3CH2OH)有3种等效氢、二甲醚(CH3OCH3)有1种等效氢,核磁共振谱可以鉴别;质谱法测相对分子质量,乙醇(CH3CH2OH)、二甲醚(CH3OCH3)相对分子质量相同,质谱法不能鉴别,乙醇(CH3CH2OH)与钠反应放出氢气,二甲醚(CH3OCH3)与钠不反应,与钠反应可以鉴别;故选C。(4)1-丙烯只有
的名称是2,2,6-三甲基-4-乙基辛烷;(3)红外光谱能测官能团,乙醇(CH3CH2OH)、二甲醚(CH3OCH3)官能团不同,红外光谱可以鉴别;核磁共振谱能测“等效氢”,乙醇(CH3CH2OH)有3种等效氢、二甲醚(CH3OCH3)有1种等效氢,核磁共振谱可以鉴别;质谱法测相对分子质量,乙醇(CH3CH2OH)、二甲醚(CH3OCH3)相对分子质量相同,质谱法不能鉴别,乙醇(CH3CH2OH)与钠反应放出氢气,二甲醚(CH3OCH3)与钠不反应,与钠反应可以鉴别;故选C。(4)1-丙烯只有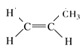 一种结构;4-辛烯有
一种结构;4-辛烯有 、
、 2种结构;1-丁烯只有
2种结构;1-丁烯只有 一种结构;2-甲基-1-丙烯只有
一种结构;2-甲基-1-丙烯只有![]() 一种结构,选B。
一种结构,选B。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案