题目内容
13.下列叙述中,错误的是( )| A. | 阿伏加德罗常数的符号为NA,其近似值为6.02×1023mol-1 | |
| B. | 等物质的量的O2与O3,所含氧原子数相同 | |
| C. | 在0.5molNa2SO4中,含有的Na+数约是6.02×1023 | |
| D. | 化合反应与分解反应可能是氧化还原反应,而复分解反应一定不是氧化还原反应 |
分析 A、阿伏伽德罗常数的单位为mol-1;
B、O2与O3分别由2个和3个氧原子构成;
C、1molNa2SO4中含2molNa+;
D、有电子得失或偏移的反应为氧化还原反应.
解答 解:A、阿伏伽德罗常数的单位为mol-1,数值为6.02×1023,故A正确;
B、O2与O3分别由2个和3个氧原子构成,故等物质的量的氧气和臭氧中含有的氧原子的个数之比为2:3,故B错误;
C、1molNa2SO4中含2molNa+,故0.5molNa2SO4中含1molNa+即6.02×1023个,故C正确;
D、有电子得失或偏移的反应为氧化还原反应,故有单质参加的化合反应、有单质生成的分解反应为氧化还原反应,而复分解反应一定不是氧化还原反应,故D正确.
故选B.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
3.往100mL 4mol/L的AlCl3溶液中滴加2mol/L的NaOH溶液,得到23.4g沉淀,则加入NaOH溶液的体积可能是( )
| A. | 300 mL | B. | 400mL | C. | 600 mL | D. | 650 mL |
1.下列有关化学用语错误的是( )
| A. | 硫离子的核外电子排布式:1s22s22p6 | |
| B. | 碳-14的原子组成符号:${\;}_{6}^{14}$C | |
| C. | 碳原子的外围电子轨道表示式: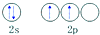 | |
| D. | Cl-的结构示意图: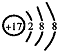 |
8.下列物质溶于水中,化学键不发生改变的是( )
| A. | 氧气 | B. | 氯化氢 | C. | 氯化钠 | D. | 氢氧化钠 |
5.下列反应的离子方程式书写正确的是( )
| A. | 稀H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 氯化铜溶液与铁粉反应:Cu2++Fe=Fe2++Cu | |
| C. | Mg与盐酸的反应:2Mg+2H+=2Mg2++H2↑ | |
| D. | 碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |