题目内容
【题目】某化学兴趣小组为研究生铁(含碳)与浓硫酸的反应情况及产物性质,设计如下实验。请回答下列问题:
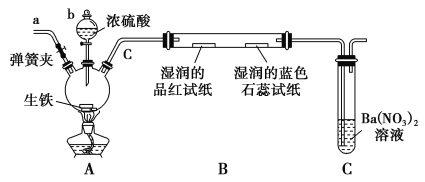
(1)按上图所示装置进行实验(夹持装置及尾气处理装置未画出)。仪器b的名称为________;实验过程中,装置B中观察的现象是______________________。
(2)装置C中有白色沉淀生成,该反应化学方程式为_______________________。
(3)装置A中还会产生CO2气体,请写出产生CO2的化学方程式:_______________________。
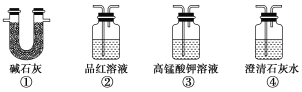
(4)为了验证装置A中产生的气体中含有CO2,应先从下列①~④中选出必要的装置连接A装置中c处管口,从左到右的顺序为________(填序号);然后再进行的操作是从a处多次鼓入N2,其目的是___________________________。
(5)某同学通过验证实验后期装置A中产生的气体中还含有H2,反应的离子方程式是____________________________。
【答案】(1)分液漏斗 品红试纸褪色,石蕊试纸变红
(2)Ba(NO3)2+3SO2+2H2O===BaSO4↓+2NO+2H2SO4(书写2个方程式也可)
(3)C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O
CO2↑+2SO2↑+2H2O
(4)③②④ 赶尽装置中的空气,防止空气的CO2影响实验
(5)Fe+2H+===Fe2++H2↑
【解析】该实验的原理为
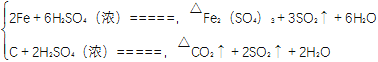 ,利用CO2和SO2的性质进行检验,(1)根据仪器的结构特点,b的名称为分液漏斗;结合SO2的化学性质,装置B中湿润的品红试纸褪色,湿润的蓝色石蕊试纸变红;(2)装置C中有白色沉淀的原因是SO2与水反应生成H2SO3,遇到Ba(NO3)2溶液被NO
,利用CO2和SO2的性质进行检验,(1)根据仪器的结构特点,b的名称为分液漏斗;结合SO2的化学性质,装置B中湿润的品红试纸褪色,湿润的蓝色石蕊试纸变红;(2)装置C中有白色沉淀的原因是SO2与水反应生成H2SO3,遇到Ba(NO3)2溶液被NO![]() 氧化为SO
氧化为SO![]() ,SO
,SO![]() +Ba2+===BaSO4↓,该反应的化学方程式为Ba(NO3)2+3SO2+2H2O===BaSO4↓+2NO+2H2SO4;(3)生铁中的炭与浓硫酸反应会产生CO2,其化学方程式为C+2H2SO4(浓)
+Ba2+===BaSO4↓,该反应的化学方程式为Ba(NO3)2+3SO2+2H2O===BaSO4↓+2NO+2H2SO4;(3)生铁中的炭与浓硫酸反应会产生CO2,其化学方程式为C+2H2SO4(浓) ![]() CO2↑+2SO2↑+2H2O;(4)检验CO2通常用澄清的石灰水,检验前要排除SO2的干扰,并保证除净,要用到KMnO4溶液和品红溶液,从左到右的顺序为③②④;由于装置中有空气,而空气中的CO2对实验有影响,应从a处多次鼓入N2,赶尽装置中的空气;(5)反应后期浓硫酸会变稀,Fe与稀H2SO4反应会产生H2,反应的离子方程式是Fe+2H+===Fe2++H2↑。
CO2↑+2SO2↑+2H2O;(4)检验CO2通常用澄清的石灰水,检验前要排除SO2的干扰,并保证除净,要用到KMnO4溶液和品红溶液,从左到右的顺序为③②④;由于装置中有空气,而空气中的CO2对实验有影响,应从a处多次鼓入N2,赶尽装置中的空气;(5)反应后期浓硫酸会变稀,Fe与稀H2SO4反应会产生H2,反应的离子方程式是Fe+2H+===Fe2++H2↑。

 阅读快车系列答案
阅读快车系列答案