题目内容
【题目】已知水在25℃和95℃时,其电离平衡曲线如图所示.
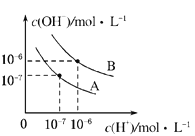
(1)95℃时水的电离平衡曲线应为______(填“A”或“B”),理由是______.
(2)曲线A所对应的温度下,pH=2的HCl溶液和pH=12的某BOH溶液中,若水的电离程度分别用α1、α2表示,则α1______α2(填“大于”、“小于”、“等于”或“无法确定”,下同),若将二者等体积混合,则混合溶液的pH______7.
(3)在曲线B所对应的温度下,将0.02molL﹣1的Ba(OH)2溶液与等物质的量浓度的NaHSO4溶液等体积混合,所得混合液的pH=______.
【答案】B水电离需要吸热,温度越高KW越大等于>或=10
【解析】试题分析:本题考查水的电离、溶液的酸碱性等,题目难度中等。利用水电离的影响因素、pH计算相关知识进行作答。
(1)曲线A条件下Kw=c(H+)c(OH-)=10-7×10-7=10-14,曲线B条件下c(H+)=c(OH-)=10-6mol/L,Kw=c(H+)c(OH-)=10-12;水的电离时吸热过程,加热促进电离,Kw增大,95℃时水的电离平衡曲线应为B。
(2)酸溶液中分析水的电离,计算溶液中氢氧根浓度;碱溶液中分析水的电离,计算溶液中氢离子浓度。曲线A所对应的温度下,pH=2的HCl溶液中氢氧根浓度为10-12mol/L;pH=12的某BOH溶液中氢离子浓度为10-12mol/L。若水的电离程度分别用α1、α2表示,则α1等于α2;若将二者等体积混合,若BOH为强碱,二者恰好完全反应,生成的NaB为强酸强碱盐,溶液呈中性,则混合溶液的pH=7;若BOH为弱碱,则碱远过量,溶液呈碱性,pH>7。
(3)95℃时,0.02molL﹣1的Ba(OH)2溶液中氢氧根浓度为0.04mol/L,0.02molL﹣1的NaHSO4溶液溶液中氢离子浓度为0.02molL﹣1,二者等体积混合,混合液中氢氧根浓度为(0.04-0.02)molL﹣1÷2=0.01 molL﹣1,95℃时,Kw= 10-12,溶液中氢离子浓度为10-10 molL﹣1,所得混合液的pH=-lgc(H+)=10。

【题目】以Al和不同的铜盐溶液间的反应为实验对象,探索Al与不同铜盐溶液反应的多样性。
实验 | 向试管中加入2ml溶液 | 实验现象 |
| 实验Ⅰ:0.5mol/LCuCl2溶液 | 15s:大量气泡且有红色物质析出 60s:反应进一步加快且反应剧烈放热,液体几乎沸腾 120s:铝片反应完,试管中析出大量蓬松的红色物质 |
实验Ⅱ:0.5mol/LCuSO4溶液 | 15s 无明显现象 60s:铝片表面有极少气泡 120s:有少量气泡溢出,铝片边缘有很少红色物质生成 |
(1)对实验Ⅰ进行研究②④
①实验Ⅰ中生成红色物质的离子方程式为:____________________________
经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:_____________________
③请写出60s后反应进一步加快可能的原因(写出两条)_____________________________
(2)对实验Ⅱ进行研究
实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42-对Al与Cu2+的置换反应存在一定的抑制作用。
假设二:________________________
(3)为进一步研究上述假设,设计如下实验:
实验 | 向试管中加入2mL溶液 | 实验现象 |
| 实验Ⅲ:0.5mol/LCuCl2溶液+1g Na2SO4固体 | 加入 Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 |
实验Ⅳ:0.5mol/L CuCl2溶液+5g Na2SO4固体 | 加入Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 | |
实验Ⅴ:0.5mol/LCuSO4溶液+0.02mol NaCl固体 | 未加入 NaCl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 | |
实验Ⅵ:0.5mol/LCuSO4溶液+_________ NH4Cl固体 | 未加入 NH4Cl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 |
_____________________________________
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:______________________________________
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:______________________________________
(4)请设计实验证明Cl-对Al与H+的反应同样起到相似的作用:_________________