题目内容
【题目】海洋是资源的宝库,醢藏着丰富的化学元素,如氯、溴、碘等,海洋资源的综合利用具有非常广阔的前景。
(1)下列说法正确的是_________。
a.AgCl、AgBr、AgI的颜色依次变深 b.F、Cl、Br、I的非金属性依次增强
c.HF、HCl、HBr、HI的还原性的依次增强 d.F2、Cl2、Br2、I2与H2化合由难变易
(2)实验室从海藻灰中提取少量碘的流程如下图:
![]()
①氧化时,可以加入MnO2在酸性条件下进行氧化,反应的离子方程式为:_________。
②上述步骤①②③分离操作分别为过滤、_________、_________。
(3)从海水提取的粗盐中含有Mg2+、Fe2+、Ca2+和SO42—等杂质,“除杂”所需试剂有:①过量的NaOH溶液②过量的Na2CO3溶液③适量的盐酸④过量的BaCl2溶液.试剂的添加顺序为_________。
为使Ca2+完全沉淀,溶液中c(CO32—)应不小于_________mol/L。[已知Ksp(CaCO3)=2.9×10-9,离子浓度小于1×10-5mol/L视为完全沉淀]
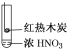
(4)目前,利用食盐制取纯碱主要有“氨碱法”和“联合制碱法”两种工艺
①能析出 NaHCO3的原因是_________。
②“氨碱法”是在滤液中加入_________产生NH3,循环使用,但产生大量的度弃物CaCl2;“联合制碱法“是在滤液中继续通入NH3,并加入NaCl粉末以制得更多的副产物_________。
③常温下,向饱和食盐水中通入NH3和CO2,当(HCO3—)=c(NH4+)时,溶液的pH_____7 (填“>”、“<”或“=”)。
【答案】ac MnO2+2I—+4H+=Mn2++I2+2H2O 分液 蒸馏 ①④②③(或④②①③或④①②③) 2.9×10-44) NaHCO3的溶解度最小 CaO[或Ca(OH)2] NH4Cl 小于
【解析】
(1) a.AgCl、AgBr、AgI的颜色分别为白色、浅黄色、黄色,依次变深;
b.F、Cl、Br、I的非金属性依次减弱,金属性依次增强;
c.HF、HCl、HBr、HI的稳定性依次减弱,即还原性的依次增强;
d.F2、Cl2、Br2、I2与H2化合由易变难;
(2)①氧化时,在酸性条件下MnO2与碘离子反应生成二价锰离子、碘单质和水;
②步骤①为固液分离,方法为过滤;②为萃取后分液;③蒸发掉有机物生成晶态碘;
(3) 除Mg2+、Fe2+用NaOH,除Ca2+用碳酸钠,除SO42-用氯化钡溶液,但会引入钡离子,除钡离子也用碳酸钠,则除硫酸根离子在除钙离子之前,过滤后再加盐酸除去碳酸根离子和氢氧根离子;根据Ksp(CaCO3)计算;
(4) ①NaHCO3的溶解度小于碳酸钠的;
②“氨碱法”滤液中的主要成分为氯化铵;
③根据溶液呈电中性计算、判断。
(1) a.AgCl、AgBr、AgI的颜色分别为白色、浅黄色、黄色,依次变深,a正确;
b.F、Cl、Br、I的非金属性依次减弱,金属性依次增强,b错误;
c.HF、HCl、HBr、HI的稳定性依次减弱,即还原性的依次增强,c正确;
d.F2、Cl2、Br2、I2与H2化合由易变难,d错误;
答案为ac;
(2)①氧化时,在酸性条件下MnO2与碘离子反应生成二价锰离子、碘单质和水,离子方程式为MnO2+2I-+4H+=Mn2++I2+2H2O;
②步骤①为固液分离,方法为过滤;②为萃取后分液;③蒸发掉有机物生成晶态碘;
(3) 除Mg2+、Fe2+用NaOH,除Ca2+用碳酸钠,除SO42-用氯化钡溶液,但会引入钡离子,除钡离子也用碳酸钠,则除硫酸根离子在除钙离子之前,过滤后再加盐酸除去碳酸根离子和氢氧根离子,添加顺序为①④②③(或④②①③或④①②③);Ksp(CaCO3)=c(Ca2+)×c(CO32-)=2.9×10-9,则c(CO32-)=2.9×10-4mol/L;
(4) ①NaHCO3的溶解度小于碳酸钠的,则饱和碳酸钠溶液中通二氧化碳和氨气时能析出碳酸氢钠;
②“氨碱法”滤液中的主要成分为氯化铵,加入CaO[或Ca(OH)2]时可产生氨气;在滤液中继续通入NH3,并加入NaCl粉末能得到更多的氯化铵;
③根据溶液呈电中性,c(Na+)+c(H+)+c(NH4+)=c(Cl-)+c(OH-)+c(HCO3-)+2c(CO32-),c(Na+)=c(Cl-),c(NH4+)=c(HCO3-),则c(H+)= c(OH-)+2c(CO32-),溶液呈酸性,pH<7。

【题目】高铁酸盐在能源、环保等方面有着广泛的用途。湿法、干法制备高铁酸盐的原理如下表所示:
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
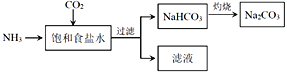
(1)工业上用湿法制备高铁酸钾(K2FeO4)的流程如图所示:
①洗涤粗品时选用异丙醇而不用水的理由是:________。
②反应II的离子方程式为___________。
③高铁酸钾在水中既能消毒杀菌,又能净水,是一种理想的水处理剂.它能消毒杀菌是因为_______它能净水的原因是_______。
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾。
①加入饱和KOH溶液的目的是:__________。
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠____(填“大”或“小”)。
(3)干法制备K2FeO4的反应中氧化剂和还原剂的物质的量之比________
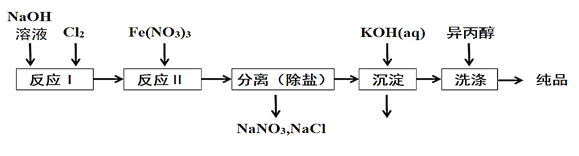
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A.由①中的红棕色气体,推断产生的气体一定是混合气体
B.红棕色气体不能表明②中木炭与浓硝酸发生了反应
C.由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D.③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应