题目内容
【题目】实验室制备硝基苯的方法是将苯与浓硫酸和浓硝酸的混合液加热到 50~60℃反应。已知苯与硝基苯的基本物理性质如下表所示:
熔点 | 沸点 | 状态 | |
苯 | 5.51℃ | 80.1℃ | 无色液体 |
硝基苯 | 5.7℃ | 210.9℃ | 油状液体 |
(1)(在大试管中)配制浓硫酸和浓硝酸的混合酸的操作方法是____________________。
(2)分离硝基苯和水的混合物的方法是________;分离硝基苯和苯的方法是_________。
(3)某同学用如图装置制取硝基苯:
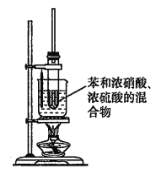
①用水浴加热的优点是________________________________________________________;
②被水浴加热的试管口部都要带一长导管,其作用是______________________________。
(4)写出此反应的化学方程式_________________________________________________。
【答案】将浓H2SO4慢慢加入浓 HNO3中,边加边振荡 分液 蒸馏 使反应体系受热均匀,容易控制温度 冷凝回流,减少苯、硝酸的挥发 ![]()
![]()
【解析】
(1)配制溶液,一般将密度大的液体加入密度小的液体中并不断搅拌;
(2)硝基苯与水互不相溶;硝基苯和苯互溶;
(3)①用水浴加热的优点是使反应体系受热均匀,容易控制温度;
②苯和浓硝酸易挥发,所以长导管的作用是冷凝回流;
(4)苯和浓硝酸、浓硫酸混合加热反应生成硝基苯。
(1)根据配制溶液的一般原则,(在大试管中)配制浓硫酸和浓硝酸的混合酸的操作方法是将浓H2SO4慢慢加入浓 HNO3中,边加边振荡;综上所述,本题答案是:将浓H2SO4慢慢加入浓 HNO3中,边加边振荡。
(2)硝基苯不溶于水,可用分液的方法分离硝基苯和水的混合物;硝基苯和苯互溶,且沸点差别较大,可用蒸馏法分离;综上所述,本题答案是:分液;蒸馏。
(3)①用水浴加热的优点是使反应体系受热均匀,容易控制温度;综上所述,本题答案是:使反应体系受热均匀,容易控制温度。
②苯和浓硝酸易挥发,故应在被水浴加热的试管口部带一长导管,其作用是冷凝回流,减少苯、硝酸的挥发;综上所述,本题答案是:冷凝回流,减少苯、硝酸的挥发。
(4)苯和浓硝酸、浓硫酸混合加热反应生成硝基苯,反应的化学方程式:![]()
![]() ;综上所述,本题答案是:
;综上所述,本题答案是:![]()
![]() 。
。

【题目】以冶炼金属铝的废弃物铝灰为原料制取超细α-氧化铝,既能降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为A12O3(含少量杂质SiO2、FeO、Fe2O3),其制备流程如下:

(1)用上图中“滤渣”和NaOH焙烧制备硅酸钠,可采用的装置为_____(填选项编号)。

(2)流程中加入H2O2有气体产生,原因是___________________________________。
(3)通过调节溶液的pH来“沉铁”,得到Fe(OH)3.已知:
Fe3+ | Fe2+ | Al3+ | |
开始沉淀时的pH | 2.2 | 7.5 | 3.7 |
完全沉淀时的pH | 3.2 | 9.0 | 4.7 |
为保证产品的纯度,可以选用下列物质中的_______调节溶液pH(填字母),调节pH的范围为______________。
a.Al2O3 b.NaOH c.Al(OH)3 d.Na2CO3
(4)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)212H2O]![]() 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置:
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置:

①集气瓶中收集到的气体是____________(填化学式)。
②装有KMnO4溶液洗气瓶的作用是____________________________。
③选用一种常用化学试剂和稀硝酸检验硫酸铝铵,该试剂_________。写出硫酸铝铵加入足量该试剂的离子方程式__________________________________________________。
④20℃时,0.1mol·L-1硫酸铝铵,其溶液pH=3,则溶液中,2c(SO42-)-c(NH4+)-3c(Al3+)=____________mol·L-1(填具体数字计算式,不必化简)





