题目内容
17.元素周期表是元素周期律的具体表现形式,根据元素周期表,人们可以发现并预测新元素和新物质,且为我们学习化学打良好的基础.如果同周期元素A、B,A位于第ⅡA族,B位于第ⅢA族.如果A的质子数为Z,则B的质子数不可能是( )| A. | Z+1 | B. | Z+11 | C. | Z+25 | D. | Z+32 |
分析 元素周期表中,从第四周期开始出现过渡元素,第ⅠA、ⅡA之后是第ⅢB,在第六、七周期中的过渡元素又出现镧系和锕系,根据周期表的结构来回答.
解答 解:因为是同一周期的IIA族,即同一横行往右一个主族,在第二、三周期原子序数增加1,因而可以Z+1;
又因为IIA族与IIIA族元素在第四周期起有过渡元素,因而又可以为Z+11;
在第六、七周期的过渡元素中又出现镧系和锕系,因而又可以为Z+25,
故选D.
点评 本题考查学生元素周期表的结构知识,注意把握周期表中的列和族的关系及副族元素的位置,题目难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目
7.下列化合物,按其晶体的熔点由高到低排列正确的是( )
| A. | CsCl、SiO2、CBr4、CF4 | B. | SiO2、CsCl、CF4、CBr4 | ||
| C. | SiO2、CsCl、CBr4、CF4 | D. | CF4、CBr4、CsCl、SiO2 |
5.化学反应的本质是旧的化学断裂新的化学键形成,即有新物质的生成,下列变化属于物理变化的是( )
| A. | 石油的分馏 | B. | 煤的干馏 | ||
| C. | 氧气变臭氧 | D. | 乙烯通入溴水,溴水褪色 |
12.目前,科学界拟合成一种“双重结构”的球形分子,即把足球烯C60的分子容纳在Si60分子中,外面的硅原子与里面的碳原子以共价键结合,下列叙述错误的是( )
| A. | 该晶体为原子晶体 | B. | 该物质的熔沸点较低 | ||
| C. | 该物质是新化合物 | D. | 该物质的相对分子量质量为2400 |
2.下列叙述正确的是( )
| A. | 1mol H2SO4的质量是98g•mol-1 | |
| B. | CO2的摩尔质量等于CO2的相对分子质量 | |
| C. | 0.012kg C-12里所含碳原子个数约为6.02×1023个 | |
| D. | 1mol任何物质的质量等于该物质的相对分子质量 |
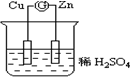 如图所示的原电池装置中,锌为负极,电极发生的是氧化反应(填氧化或还原),电极反应式为Zn-2e-=Zn2+;铜电极反应式为2H++2e-=H2↑,铜片上观察到的现象为有气泡产生.
如图所示的原电池装置中,锌为负极,电极发生的是氧化反应(填氧化或还原),电极反应式为Zn-2e-=Zn2+;铜电极反应式为2H++2e-=H2↑,铜片上观察到的现象为有气泡产生.