题目内容
4.某学生用化学知识解决生活中的问题,下列家庭小实验或说法不合理的是( )| A. | 用食醋除去暖水瓶中的薄层水垢 | |
| B. | 用米汤检验食盐中是否含碘酸钾(KIO3) | |
| C. | 医用酒精的浓度通常为75%,可用于杀菌消毒 | |
| D. | 用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物 |
分析 A.醋酸含有羧基,可与碳酸钙反应;
B.淀粉与碘发生反应;
C.医用酒精可使蛋白质变性;
D.纯羊毛织物的主要成分为蛋白质,根据蛋白质的性质判断.
解答 解:A.醋酸含有羧基,酸性比碳酸强,可与碳酸钙反应,故A正确;
B.淀粉与碘发生反应,与碘酸钾不反应,故B错误;
C.医用酒精可使蛋白质变性,可用于杀菌消毒,故C正确;
D.纯羊毛织物的主要成分为蛋白质,灼烧具有烧焦的羽毛气味,可用于检验蛋白质,故D正确.
故选B.
点评 本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力的考查,题目有利于培养学生的良好的科学素养,难度不大.

练习册系列答案
相关题目
14.某溶液中含有HCO${\;}_{3}^{-}$,SO${\;}_{3}^{2-}$,CO${\;}_{3}^{2-}$,CH3COO-等四种阴离子,向其中加入足量的Na2O2固体后,假设溶液体积无变化,溶液中离子浓度基本保持不变的是( )
| A. | CO${\;}_{3}^{2-}$ | B. | HCO${\;}_{3}^{-}$ | C. | CH3COO- | D. | SO${\;}_{3}^{2-}$ |
12.普洱是我国著名的茶叶产地,“普洱茶”香飘四海.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压、提高记忆力、保护神经细胞等.下列有关茶氨酸的说法中,错误的是( )
| A. | 茶氨酸由C、H、O、N四种元素组成 | |
| B. | 每个茶氨酸分子含有26个原子 | |
| C. | 茶氨酸中碳元素与氢元素的质量比为6:1 | |
| D. | 每个茶氨酸分子中含有1个N2分子 |
19.乙酸与乙酸乙酯的混合物中H元素的质量分数是$\frac{1}{11}$,则O元素的质量分数是( )
| A. | $\frac{10}{11}$ | B. | $\frac{7}{11}$ | C. | $\frac{6}{11}$ | D. | $\frac{4}{11}$ |
9.下列实验叙述有错误的是( )
| A. | 实验室制取乙烯气体时,将温度计的水银球放入液面以下 | |
| B. | 向淀粉水解后的溶液中加入碘水,溶液变蓝,证明淀粉尚未水解 | |
| C. | 证明分子CH2=CH-CHO既含有醛基又含有C=C,可先向溶液中先加入足量的银氨溶液加热,充分反应后,再加入足量的溴水 | |
| D. | 在蔗糖与稀硫酸共热后的溶液中,滴加银氨溶液,验证产物中的葡萄糖 | |
| E. | 用新制的银氨溶液可区分甲酸甲酯和乙醛 |
14.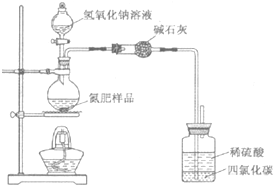 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
氢氧化钠少量时2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O
氢氧化钠过量时NH4HSO4+2NaOH=Na2SO4+NH3↑+2H2O
(1)同学们设计的实验装置图如下,请回答相关问题.
①装置中碱石灰的作用是吸收氨气中的水蒸气.
②广口瓶内四氯化碳的作用是防止倒吸.
③指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外逸,测得的样品含氮量仍将偏低,其原因可能是残留在反应装置中的氨气未被稀硫酸吸收.
(2)同学们改进实验装置后(改进装置图略),进行如下实验.称取不同质量的上述样品分别与40.00mL相同浓度的氢氧化钠溶液混合,完全溶解后,加热充分反应(此温度下铵盐不分解),并使生成的氨气全部被稀硫酸吸收,测得氨气的质量.部分实验数据如下:
请计算(计算结果保留两位小数):
①样品中氮元素的质量分数是19.87%.
②所用氢氧化钠溶液的物质的量浓度为3.25 mol/L.
③若样品质量为31.00g,则生成氨气的质量为1.53 g.
 某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:
某氮肥硫酸铵中混有硫酸氢铵.为测定该氮肥的含氮量,一化学研究性学习小组取一定量氮肥样品,研磨使其混合均匀,备用.已知:氢氧化钠少量时2NH4HSO4+2NaOH=(NH4)2SO4+Na2SO4+2H2O
氢氧化钠过量时NH4HSO4+2NaOH=Na2SO4+NH3↑+2H2O
(1)同学们设计的实验装置图如下,请回答相关问题.
①装置中碱石灰的作用是吸收氨气中的水蒸气.
②广口瓶内四氯化碳的作用是防止倒吸.
③指导老师指出,用该装置进行实验,即使氢氧化钠足量且实验过程中无氨气外逸,测得的样品含氮量仍将偏低,其原因可能是残留在反应装置中的氨气未被稀硫酸吸收.
(2)同学们改进实验装置后(改进装置图略),进行如下实验.称取不同质量的上述样品分别与40.00mL相同浓度的氢氧化钠溶液混合,完全溶解后,加热充分反应(此温度下铵盐不分解),并使生成的氨气全部被稀硫酸吸收,测得氨气的质量.部分实验数据如下:
| 氢氧化钠溶液/mL | 40.00 | ||
| 样品质量/g | 7.750 | 15.50 | 23.25 |
| 氨气质量/g | 1.870 | 1.870 | 1.700 |
①样品中氮元素的质量分数是19.87%.
②所用氢氧化钠溶液的物质的量浓度为3.25 mol/L.
③若样品质量为31.00g,则生成氨气的质量为1.53 g.
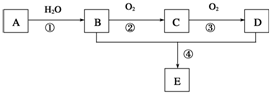 已知①A是一种分子量为28的气态烃,②2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.请回答下列问题:
已知①A是一种分子量为28的气态烃,②2CH3CHO+O2$→_{△}^{催化剂}$2CH3COOH,现以A为主要原料合成一种具有果香味的物质E,其合成路线如图所示.请回答下列问题: ,B分子中的官能团名称羟基.
,B分子中的官能团名称羟基.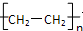 .
.