题目内容
17.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )| A. | 标准状况下,2.24 L苯中含有的分子数为0.1 NA | |
| B. | 标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1 NA | |
| C. | 0.1 mol•L-1的硫酸铜溶液中含铜离子数为0.1 NA | |
| D. | 1mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
分析 A.标况下苯为液态;
B.从氯气的自身氧化还原反应来分析计算电子转移数;
C.溶液体积未知,无法计算;
D.氢氧化铁胶体胶粒是氢氧化铁的集合体.
解答 解:A.标况下苯为液态,不能使用气体摩尔体积,故A错误;
B.2.24LCl2与过量稀NaOH溶液反应,Cl2+2NaOH=NaCl+NaClO+H2O,每1mol氯气反应电子转移数为1mol,则0.1molCl2与氢氧化钠反应转移电子为0.1mol,即0.1NA,故B正确;
C.溶液体积未知,无法计算铜离子的数目,故C错误;
D.1mol FeCl3完全水解转化为氢氧化铁胶体,氢氧化铁胶体微粒是氢氧化铁的集合体,生成胶粒小于NA个,故D错误;
故选:B.
点评 本题考查了阿伏伽德罗常数的综合应用,熟练掌握物质的量与阿伏伽德罗常数、摩尔质量等物理量之间的关系为解答关键,注意气体摩尔体积的使用条件,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.如表为烯类化合物与溴发生加成反应的相对速率(以乙烯为标准).
(1)下列化合物与氯化氢加成时,取代基对速率的影响与表中规律类似,其中反应速率最快的是A(填序号).
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3 C.CH2=CH CH3 D.CH2=CHCl
该物质的名称为2,3-二甲基-2-丁烯
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2Br(次要产物)
请写出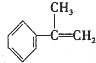 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式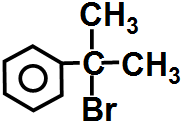 .
.
| 烯类化合物 | 相对速率 |
| (CH3)2C=CHCH3 | 10.4 |
| CH3CH=CH2 | 2.03 |
| CH2=CH2 | 1.00 |
| CH2=CHBr | 0.04 |
A.(CH3)2C=C(CH3)2 B.CH3CH=CHCH2CH3 C.CH2=CH CH3 D.CH2=CHCl
该物质的名称为2,3-二甲基-2-丁烯
(2)烯烃与溴化氢、水加成时,产物有主次之分,例如:CH2=CHCH3+HBr→CH3CHBrCH3(主要产物)+CH3CH2Br(次要产物)
请写出
 与HBr反应的主要产物的结构简式
与HBr反应的主要产物的结构简式 .
.
12.下列对于过氧化钠的叙述中,正确的是( )
| A. | 78g过氧化钠中含阴离子2mol | |
| B. | 过氧化钠能与水反应,所以过氧化钠可以作很多气体的干燥剂 | |
| C. | 过氧化钠与水反应时,过氧化钠是氧化剂,水是还原剂 | |
| D. | 过氧化钠与二氧化碳反应时,过氧化钠既是氧化剂又是还原剂 |
2.下列叙述中,不属于氮的固定的方法是( )
| A. | 根瘤菌把氮气变为硝酸盐 | B. | 氮气和氢气合成氨 | ||
| C. | 从液态空气中分离氮气 | D. | 氮气和氧气合成一氧化氮 |
6.下列各项关系中正确的是( )
| A. | 原子半径:Al>Mg>F | B. | 结合质子能力:OH->CH3COO->Cl- | ||
| C. | 热稳定性:HF>H2S>H2O | D. | 碱性:NaOH>KOH>Mg(OH)2 |
 .
.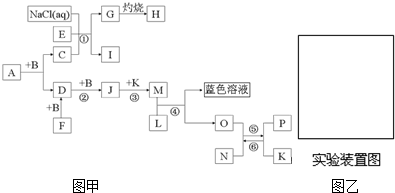
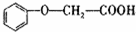 发生酯化反应的产物A是一种食用香料;11.6g甲完全燃烧可产生0.6mo1CO2和0.6mo 1H2O.相同条件下,甲蒸气对氧气的相对密度为1.8125,甲分子为链状结构且不含甲基.
发生酯化反应的产物A是一种食用香料;11.6g甲完全燃烧可产生0.6mo1CO2和0.6mo 1H2O.相同条件下,甲蒸气对氧气的相对密度为1.8125,甲分子为链状结构且不含甲基.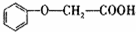 生成A的化学方程式为
生成A的化学方程式为  $?_{△}^{浓H_{2}SO_{4}}$
$?_{△}^{浓H_{2}SO_{4}}$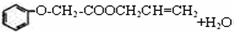 .
.