题目内容
7.钙和氢气在一定温度下可化合反应生成一种灰白色的化合物A(金属氢化物).该化合物在熔融状态下能导电.取少量A投放水中剧烈反应放出一种无色无味气体,并形成一种碱溶液.(1)钙和氢气反应的化学方程式:Ca+H2═CaH2,其中H2作氧化剂.化合物A中氢元素的化合价为-1价.
(2)化合物A与水反应的化学方程式为:CaH2+2H2O═Ca(OH)2+2H2↑,其中A作还原剂.
分析 (1)Ca与氢气反应生成CaH2,H2得电子化合价降低作氧化剂,根据钙元素的化合价判断;
(2)CaH2与H2O反应生成Ca(OH)2、H2,CaH2中H元素的化合价升高.
解答 解:(1)Ca与氢气反应生成CaH2,该反应为Ca+H2═CaH2,H元素的化合价降低,则H2作氧化剂,CaH2中Ca元素的化合价为+2价,则H为-1价;
故答案为:Ca+H2═CaH2;氧化;-1;
(2)CaH2与H2O反应生成Ca(OH)2、H2,钙反应为CaH2+2H2O═Ca(OH)2+2H2,↑,CaH2中H元素的化合价升高,则A作还原剂,
故答案为:CaH2+2H2O═Ca(OH)2+2H2↑;还原.
点评 本题考查氧化还原反应,把握反应中元素的化合价变化为解答的关键,注重知识迁移应用能力的考查,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
17.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 标准状况下,2.24 L苯中含有的分子数为0.1 NA | |
| B. | 标准状况下,2.24 L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.1 NA | |
| C. | 0.1 mol•L-1的硫酸铜溶液中含铜离子数为0.1 NA | |
| D. | 1mol FeCl3跟水完全反应转化为氢氧化铁胶体后,其中胶体粒子的数目为NA |
18.常温下,以下三种物质度积常数为:Ksp[Mg(OH)2]=1.2×10-11、Ksp(AgCl)=1.8×10-10、Ksp(Ag2CrO4)=8.3×10-9.下列说法正确的是( )
| A. | 温度升高,Ksp(AgCl)不变 | |
| B. | 向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)变大 | |
| C. | 常温下,将0.001 mol•L-1 AgNO3溶液滴入0.001 mol•L-1 KCl和 0.001 mol•L-1 K2CrO4溶液先产生Ag2CrO4沉淀 | |
| D. | 在Mg2+为0.12 mol•L-1的溶液中要产生Mg(OH)2沉淀,应控制溶液的pH>9 |
15.下列实验操作或描述正确的是( )
| A. | 焰色反应实验中,铂丝在蘸取待测溶液前,应先用稀硫酸洗净并灼烧 | |
| B. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 取用一小块钾后,剩余的钾可放回原试剂瓶里 | |
| D. | 将NaOH溶液滴加到AlCl3溶液中,振荡,制备Al(OH)3胶体 |
2.下列物质属于电解质的是( )
| A. | CO2 | B. | H2SO4溶液 | C. | BaSO4 | D. | NaOH溶液 |
4. 为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如右图所示.下列叙述中正确的是( )
为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如右图所示.下列叙述中正确的是( )
 为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如右图所示.下列叙述中正确的是( )
为实现2008北京“科技奥运”战略,我国兴奋剂检测生物芯片装置已定型和批量生产,可快捷检测常见的16种兴奋剂.已知某兴奋剂乙基雌烯醇(etylestrenol)的结构如右图所示.下列叙述中正确的是( )| A. | 该物质可以视为烃类 | B. | 该有机物的分子式为C20H32O | ||
| C. | 不能使溴的四氯化碳溶液褪色 | D. | 该物质分子中的所有碳原子均共面 |
11.下列物质既能发生消去反应生成相应的烯烃,又能氧化成相应的醛的是( )
| A. | CH3OH | B. | CH2OHCH2CH3 | C. | (CH3)2COHCH3 | D. | (CH3)3COH |
9.在一个密闭容器中充入一种气态烃和足量的氧气,用电火花点燃,完全燃烧后,容器内气体体积保持不变(均在120℃和相同的压强下测定),这种气态烃可能是( )
| A. | CH4 | B. | C2H6 | C. | C2H4 | D. | C3H6 |
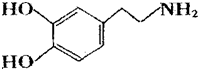
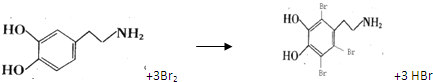 .
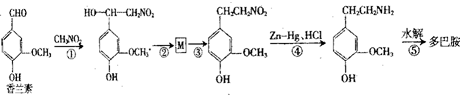
.
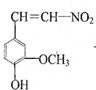 .
.