题目内容
一定条件下,体积为10L的密闭容器中,1mol X和1mol Y进行反应:2X(g)+Y(g)?Z(g)(正反应为放热反应),经60s达到平衡,生成0.3mol Z.下列说法正确的是( )
分析:A、根据v=
计算v(Z),再根据速率之比等于化学计量数之比计算v(X);
B、根据勒夏特列原理分析;
C、先计算出参加反应的Y的物质的量,再利用转化率的定义计算Y的转化率;
D、升高温度平衡向吸热方向移动.
| △c |
| △t |
B、根据勒夏特列原理分析;
C、先计算出参加反应的Y的物质的量,再利用转化率的定义计算Y的转化率;
D、升高温度平衡向吸热方向移动.
解答:解:A、v(Z)=
=0.0005mol(L?S),率之比等于化学计量数之比,所以v(X)=2v(Z)=2×0.0005mol(L?S)=0.001mol(L?S),故A正确;
B、减少X的浓度,平衡向着减弱这种改变的方向移动,即向逆反应方向移动,故B正确;
C、参加反应的Y的物质的量n(Y)=n(Z)=0.3mol,所以Y的转化率为
×100%=30%,故C错误;
D、该反应正反应为放热反应,升高温度,平衡向吸热方向移动,即向逆反应移动,故D错误;
故选AB.
| ||
| 60s |
B、减少X的浓度,平衡向着减弱这种改变的方向移动,即向逆反应方向移动,故B正确;
C、参加反应的Y的物质的量n(Y)=n(Z)=0.3mol,所以Y的转化率为
| 0.3mol |
| 1mol |
D、该反应正反应为放热反应,升高温度,平衡向吸热方向移动,即向逆反应移动,故D错误;
故选AB.
点评:本题考查化学平衡问题,题目难度不大,本题注意外界条件对化学平衡的影响,根据定义法及化学计量法计算反应速率.

练习册系列答案
相关题目
工业上制备合成气的工艺主要是水蒸气重整甲烷:CH4(g)+H2O(g) CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )
CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )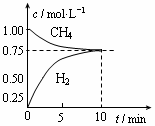
| A.10min时用CH4表示的反应速率为0.075 mol?L-1?min-1 |
| B.使用高效催化剂能够增大CO的产率 |
| C.该条件下反应的平衡常数为0.1875 |
D.升高温度能使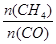 增大 增大 |

 CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )
CO(g)+3H2(g);△H=+206 kJ/mol,一定条件下向体积为1 L的密闭容器中充入1 mol CH4和1 mol H2O,测得CH4(g)和CO(g)的浓度随时间变化曲线如图所示,下列说法正确的是 ( )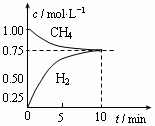
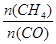 增大
增大