题目内容
把pH=2的H2SO4和pH=11的NaOH溶液混和,混和液pH=7。则两溶液的体积比是( )
| A.10:1 | B.1:10 | C.1:2 | D.2:1 |
B
试题分析:混合后溶液的pH=7,所以氢离子的物质的量等于OH-的物质的量,即
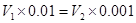 ,解得
,解得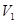 ︰
︰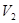 =1:10,答案选B。
=1:10,答案选B。点评:在计算溶液的pH时,如果是酸和碱反应,则首先要判断酸和碱的过量问题,如果酸过量,则首先计算溶液中氢离子浓度。如果是碱过量,则首先计算的是溶液中OH-的浓度,然后根据水的离子积常数在换算成氢离子浓度。

练习册系列答案
相关题目