��Ŀ����
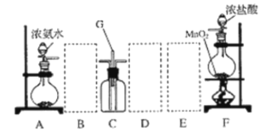
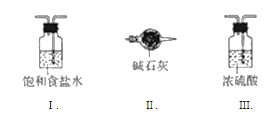
����Ŀ������ A �Ļ�ѧʽΪ NH5����������ԭ�ӵ�����㶼������Ӧ��ϡ������ԭ�ӵ��������ӽṹ���������й�˵������ȷ���ǣ� ��
A.NH5 �м��й��ۼ��������Ӽ���NH5 �����ӻ�����
B.1 mol NH5 �к��� 5NA �� N��H ����NA ��ʾ�����ӵ�������
C.NH5 �ĵ���ʽΪ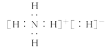
D.A ��ˮ��Ӧ�Ļ�ѧ����ʽΪ NH5��H2O=NH3��H2O��H2��
���𰸡�B
��������
A��![]() ���й��ۼ�����
���й��ۼ�����![]() ��
��![]() ֮�������Ӽ������
֮�������Ӽ������![]() Ҳ��һ�����ӻ����A����ȷ��
Ҳ��һ�����ӻ����A����ȷ��
B��![]() ��
��![]() ֮�������Ӽ������1��
֮�������Ӽ������1��![]() ������ֻ��4��
������ֻ��4��![]() ����B�����
����B�����
C����ԭ���������5�����ӣ���4����ԭ�ӳɼ�����ʧȥ1�����ӣ��պôﵽ8���ӵ��ȶ��ṹ����![]() ���õ�1�����Ӻ����ԭ�ӣ�ע���������Ӷ�Ҫ�������ţ�C����ȷ��
���õ�1�����Ӻ����ԭ�ӣ�ע���������Ӷ�Ҫ�������ţ�C����ȷ��
D��![]() ����һ��-1�۵��⣬��������ˮ��+1�۵��ⷢ�����з�Ӧ�õ���������
����һ��-1�۵��⣬��������ˮ��+1�۵��ⷢ�����з�Ӧ�õ���������![]() ���Ϊһˮ�ϰ���D����ȷ��
���Ϊһˮ�ϰ���D����ȷ��
��ѡB��

����Ŀ����������������������������ɵ���Ⱦ��Ŀǰ�о�����Ҫ���⡣
(1)��ҵ�ϳ��û���̿��ԭһ���������䷴ӦΪ��2NO(g)+C(s)![]() N2(g)+CO2(g)�����ݻ���ΪlL�ļס��ҡ����������ݺ��������зֱ���������Ļ���̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
N2(g)+CO2(g)�����ݻ���ΪlL�ļס��ҡ����������ݺ��������зֱ���������Ļ���̿��һ������NO����ø�������n(NO)�淴Ӧʱ��t�ı仯������±���ʾ��
t/min n(NO)/mol T | 0 | 40 | 80 | 120 | 160 | |
�� | T�� | 2 | 1.45 | 1 | 1 | 1 |
�� | 400�� | 2 | 1.5 | 1.1 | 0.8 | 0.8 |
�� | 400�� | 1 | 0.8 | 0.65 | 0.53 | 0.45 |
�ټ�������Ӧ�¶�T��__400��(����>������<������=��)��
���������У�0��40min��ƽ����Ӧ����v(N2)=__��
�۱������д�ƽ���NO��ת����Ϊ__��
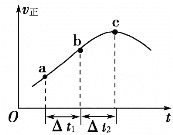
(2)����̿��ԭNO2�ķ�ӦΪ��2NO2(g)+2C(s)![]() N2(g)+2CO2(g)���ں��������£�lmolNO2����������̿�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��
N2(g)+2CO2(g)���ں��������£�lmolNO2����������̿�����÷�Ӧ�����ƽ��ʱNO2��CO2�����ʵ���Ũ����ƽ����ѹ�Ĺ�ϵ��ͼ��ʾ��

��A��B��C������NO2��ת������ߵ���__��(����A������B������C��)��
�ڼ���C��ʱ�÷�Ӧ��ѹǿƽ�ⳣ��KP=__MPa(Kp����ƽ���ѹ����ƽ��Ũ�ȼ��㣬��ѹ=��ѹ�����ʵ�������)��
(3)ȼú�������������·�����
�����٣����������Ƚ���(��Ҫ�ɷ�CO��CH4��H2)��SO2�ڸ����»�ԭ�ɵ������漰�IJ��ַ�Ӧ���£�
2CO(g)+SO2(g)=S(g)+2CO2(g) ��H1=8.0kJ��mol-1
2CO(g)+O2(g)=2CO2(g) ��H2=��566.0kJ��mol-1
2H2(g)+O2(g)=2H2O(g) ��H3=��483.6kJ��mol-1
��H2(g)��ԭSO2(g)����S(g)��H2O(g)���Ȼ�ѧ����ʽΪ__��
�����ڣ��ð�ˮ��SO2ת��ΪNH4HSO3����������(NH4)2SO4�����ð�ˮ��SO2ת��ΪNH4HSO3�����ӷ���ʽΪ__��ʵ����NH4HSO3��Һ��![]() =15������Һ��pHΪ__��(��֪��H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)
=15������Һ��pHΪ__��(��֪��H2SO3��Ka1=1.5��10-2��Ka2=1.0��10-7)