题目内容
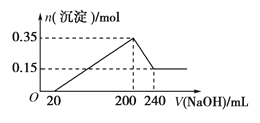
【题目】取20 mL pH=3的CH3COOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电性变化如图,则加入氨水前CH3COOH的电离度为

A. 0.5% B. 1.5% C. 0.1% D. 1%
【答案】D
【解析】
根据图象分析,当氨水的体积为10 mL时导电性最强,说明刚好与醋酸完全反应,所以醋酸的浓度为:![]() =0.1mol/L,再根据pH=3的CH3COOH溶液,则氢离子浓度为:10-3mol/L,所以CH3COOH的电离度为=(已电离的电解质的物质的量/原来总的物质的量)
=0.1mol/L,再根据pH=3的CH3COOH溶液,则氢离子浓度为:10-3mol/L,所以CH3COOH的电离度为=(已电离的电解质的物质的量/原来总的物质的量)![]() 100%进行计算。
100%进行计算。
根据图象分析,当氨水的体积为10 mL时导电性最强,说明刚好与醋酸完全反应,所以醋酸的浓度为:![]() =0.1mol/L,再根据pH=3的CH3COOH溶液,则氢离子浓度为:10-3mol/L,所以CH3COOH的电离度为
=0.1mol/L,再根据pH=3的CH3COOH溶液,则氢离子浓度为:10-3mol/L,所以CH3COOH的电离度为![]() 100%=1%,
100%=1%,
所以D选项是正确的。

【题目】中国科学家用金属钠和CO2在一定条件下制得了金刚石:4 Na + 3CO2![]() 2 Na2CO3 + C(金刚石),以下是一些物质的熔沸点数据(常压):
2 Na2CO3 + C(金刚石),以下是一些物质的熔沸点数据(常压):
钠 | Na2CO3 | 金刚石 | 石墨 | |
熔点(℃) | 97.8 | 851 | 3550 | 3850 |
沸点(℃) | 882.9 | 1850(分解产生CO2) | ---- | 4250 |
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式_____________________,若3v正(Na)=4v逆(CO2),则_____(选填序号)。
a.反应肯定达到平衡 b.反应可能达到平衡 c.反应肯定未达平衡
(2)若反应在10L密闭容器、常压下进行,5min内,测得金刚石的质量增加了6 g,该时间段内v(CO2)=______________,若反应温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将________(选填“增大”、“减小”或“不变”) 。
(3)反应中还有石墨生成,已知:C(石墨)![]() C(金刚石),若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是_________反应(填“吸热”或“放热”)。
C(金刚石),若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是_________反应(填“吸热”或“放热”)。
(4)碳酸钠溶液中滴入盐酸的反应过程如右图所示,反应至A点时,未产生二氧化碳,请用离子方程式解释原因:_________________,继续滴加盐酸,反应至B点,B点溶液中溶质的化学式是__________。

【题目】(1)K2Cr2O7的水溶液中存在如下平衡:
Cr2O72-(aq)+ H2O(l)![]() 2CrO42-(aq)+ 2H+(aq),平衡常数表达式__________
2CrO42-(aq)+ 2H+(aq),平衡常数表达式__________
已知:(在水溶液中K2Cr2O7为橙红色,K2CrO4为黄色)往上述溶液中加入氢氧化钠,溶液呈___色;向已加入氢氧化钠的溶液中,再加入过量硫酸,溶液呈___________色。
(2)在KMnO4与H2C2O4反应中,可通过测定_________________来测定该反应的速率;写出酸性条件下KMnO4与H2C2O4(弱酸)反应,产生二氧化碳气体、水和Mn2+的离子反应方程式:__________________;此反应开始反应缓慢,随后反应迅速加快,其原因是______(填字母)
A.KMnO4溶液中的H+起催化作用
B.生成的CO2逸出,使生成物浓度降低
C.反应中,生成的Mn2+起催化作用
D.在酸性条件下KMnO4的氧化性增强
(3)为探讨化学反应速率的影响因素,设计的实验方案如下表。
(已知 I2+2S2O32-===S4O62-+2I-,其中Na2S2O3溶液均足量)
实验 序号 | 体积V/mL | 时间/s | |||
Na2S2O3溶液 | 淀粉溶液 | 碘水 | 水 | ||
① | 10.0 | 2.0 | 4.0 | 0.0 | t1 |
② | 8.0 | 2.0 | 4.0 | 2.0 | t2 |
③ | 6.0 | 2.0 | 4.0 | Vx | t3 |
①该实验进行的目的是_____________
②表中Vx=_______mL,比较t1、t2、t3大小____________.