题目内容
【题目】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
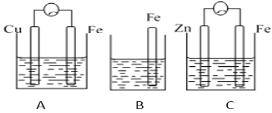
(1) B中反应的离子方程式为______。
(2) A中作正极的金属是_____,该电极上看到的现象为_____。
(3) C中作负极的金属是____,该电极反应方程式为______。
(4)现有未知金属A,将A与Fe用导线相连后放入稀硫酸溶液中,观察到A上有气泡,在A上发生____反应。(填“氧化”或“还原”)。
【答案】Fe+2H+=Fe2++H2↑ Cu 有气泡产生 Zn Zn-2e-=Zn2+ 还原
【解析】
(1) B中是铁和稀硫酸反应,故其离子方程式为Fe+2H+=Fe2++H2↑,故答案为Fe+2H+=Fe2++H2↑;
(2) A中铁比铜活泼,故铁作负极,铜作正极,该原电池正极上看到的现象为有气泡产生,故答案为:Cu;有气泡产生;
(3) C中锌比铁更活泼,故锌作负极,负极上通常是电极本身失电子被氧化,故电极反应方程式为Zn-2e-=Zn2+,故答案为:Zn-2e-=Zn2+;
(4)观察到A上有气泡,故A上发生电极反应为![]() ,故为还原反应,故答案为:还原 。
,故为还原反应,故答案为:还原 。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目