题目内容
【题目】如图为实验室某浓盐酸试剂瓶标签上的有关数据,试根据标签上的有关数据回答下列问题。
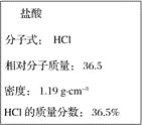
(1)该浓盐酸中HCl的物质的量浓度为__________molL﹣1。
(2)取用任意体积的该盐酸时,下列物理量中不随所取体积的多少而变化的是_________。
A.溶液中HCl的物质的量
B.溶液的浓度
C.溶液中Cl﹣的数目
D.溶液的密度
(3)配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次,并在操作步骤空白处填上适当仪器名称)_________。
A.用30 mL水洗涤__2~3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需的浓盐酸的体积,沿玻璃棒倒入烧杯中,再加入少量水(约30 mL),用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入容量瓶中
D.将容量瓶盖紧,振荡,摇匀
E.改用__加水,使溶液凹液面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1~2 cm处
(4)在配制过程中,下列实验操作对所配制的稀盐酸的物质的量浓度有何影响?(在括号内填A表示“偏大”,填B表示“偏小”,填C表示“无影响”)
a.用量筒量取浓盐酸时俯视观察凹液面__;
b.定容后经振荡、摇匀、静置,发现液面下降,再加适量的蒸馏水_________。
【答案】11.9 BD BCAFED 烧杯内壁和玻璃棒 胶头滴管 B B
【解析】
(1)根据c(HCl)=1000ρω/M计算;
(2)A.溶液中HCl的物质的量,n=c×V,溶液体积增大,HCl的物质的量增大;
B.溶液的浓度为恒定参数,不随体积的改变而改变;
C.溶液中Cl﹣的数目,N=c×V×NA,溶液体积增大,Cl﹣的数目增大;
D.溶液的密度为恒定参数,不随体积的改变而改变;
(3)配制溶液时,按先后顺序为:计算、称量、稀释、冷却、移液、洗涤、定容、摇匀;
(4)根据c=![]() ×
×![]() 判断。
判断。
(1)c(HCl)=1000ρω/M=1000×1.19×36.5%/36.5=11.9mol/L;
(2)A.溶液中HCl的物质的量,n=c×V,溶液体积增大,HCl的物质的量增大,与题意不符,A错误;
B.溶液的浓度为恒定参数,不随体积的改变而改变,符合题意,B正确;
C.溶液中Cl﹣的数目,N=c×V×NA,溶液体积增大,Cl﹣的数目增大,与题意不符,C错误;
D.溶液的密度为恒定参数,不随体积的改变而改变,符合题意,D正确;
答案为BD;
(3)配制溶液时,按先后顺序为:计算、称量、稀释、冷却、移液、洗涤、定容、摇匀,操作顺序为BCAFED;A操作为洗涤玻璃棒及烧杯内壁;E操作胶头滴管滴加蒸馏水;
(4)a.俯视观察凹液面导致读出浓盐酸的体积偏大,盐酸的物质的量偏小,配置溶液浓度偏小;
b.摇匀、静置,发现液面下降,再加适量的蒸馏水,导致溶液体积偏大,配置溶液浓度偏小。

 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案【题目】室温下,某一元弱酸HA的电离常数K=1.6×10-6。 向20.00 mL 浓度约为0.1 mol·L-1 HA溶液中逐滴加入0.1000 mol·L-1 的标准NaOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:(已知lg4=0.6)
(1)a点溶液中pH约为________,此时溶液中H2O电离出的c(H+)为________。
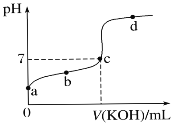
(2)a、b、c、d四点中水的电离程度最大的是________点,滴定过程中宜选用__________作指示剂,滴定终点在________(填“c点以上”或“c点以下”)。
(3)滴定过程中部分操作如下,下列各操作使测量结果偏高的是_________________(填字母序号)。
A.滴定前碱式滴定管未用标准NaOH溶液润洗
B.用蒸馏水洗净锥形瓶后,立即装入HA溶液后进行滴定
C.滴定过程中,溶液出现变色后,立即停止滴定
D.滴定结束后,仰视液面,读取NaOH溶液体积
(4)若重复三次滴定实验的数据如下表所示,计算滴定所测HA溶液的物质的量浓度为_____mol/L。
实验序号 | NaOH溶液体积/mL | 待测HA溶液体积/mL |
1 | 21.01 | 20.00 |
2 | 20.99 | 20.00 |
3 | 21.60 | 20.00 |