题目内容
【题目】实验室用燃烧法测定某固体有机物A的分子组成,测定装置如图所示(铁架台、铁夹、酒精灯等未画出):
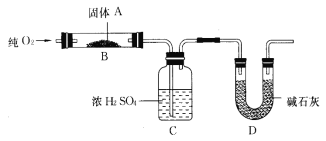
取17.1 g A放入B装置中,持续通入过量O2燃烧,生成CO2和H2O,请回答下列有关问题:
(1)通入过量O2的目的是_______________________________;
(2) D装置的作用是______________________________,有同学认为该套装置有明显的缺陷,需要改进,该同学判断的理由是___________________________;
(3)通过该实验,能否确定A中是否含有氧元素,其理由?_____________________________ ;
(4)若A的摩尔质量为342 g/mol,C装置增重9.9 g,D装置增重26.4 g,则A的分子式为______________________________;
(5)A可发生水解反应,1 mol A可水解生成2 mol同分异构体,则A在催化剂作用下水解的化学方程式为_______________________________。
【答案】使有机物A充分燃烧吸收A燃烧后生成的CO2D装置中的碱石灰可以吸收空气中的水和二氧化碳,对生成的二氧化碳质量测定有干扰能确定;如果碳元素的质量和氢元素的质量小于17.1g,则有氧元素C12H22O11C12H22O11(蔗糖)+H2O ![]() C6H12O6(葡萄糖)+C6H12O6(果糖)
C6H12O6(葡萄糖)+C6H12O6(果糖)
【解析】
(1)燃烧法测定某固体有机物A的分子组成,要通入过量O2使有机物在氧气中充分燃烧生成二氧化碳和水;故答案为:使有机物A充分燃烧;
(2)C装置中的试剂为浓硫酸,用于吸收有机物燃烧生成的水,D装置中的试剂是碱石灰用于吸收有机物燃烧生成的二氧化碳;D装置中的碱石灰可以吸收空气中的水和二氧化碳,对生成的二氧化碳质量测定有干扰,因此该套装置需要改进,故答案为:吸收A燃烧后生成的CO2;D装置中的碱石灰可以吸收空气中的水和二氧化碳,对生成的二氧化碳质量测定有干扰;
(3)通过浓硫酸增重的质量可以求出有机物中氢的质量,通过碱石灰增重的质量可以求出有机物中碳的质量,再根据A的质量判断是否有氧元素;故答案为:能确定,如果碳元素的质量和氢元素的质量小于17.1g,则有氧元素;
(4)浓硫酸增重可知水的质量为9.9g,可计算出n(H2O)=![]() =0.55mol,n(H)=1.1mol,m(H)=1.1g;使碱石灰增重26.4g,可知二氧化碳质量为26.4g,n(C)=n(CO2)=
=0.55mol,n(H)=1.1mol,m(H)=1.1g;使碱石灰增重26.4g,可知二氧化碳质量为26.4g,n(C)=n(CO2)=![]() =0.6mol,m(C)=7.2g,m(C)+m(H)=8.31g,有机物的质量为17.1g,所以有机物中氧的质量为8.79g,n(O)=
=0.6mol,m(C)=7.2g,m(C)+m(H)=8.31g,有机物的质量为17.1g,所以有机物中氧的质量为8.79g,n(O)=![]() =0.55mol,n(C):n(H):n(O)=0.6mol:1.1mol:0.55mol=12:22:11,即实验式为C12H22O11,A的摩尔质量为342g/mol,所以分子式也为C12H22O11,故答案为:C12H22O11;
=0.55mol,n(C):n(H):n(O)=0.6mol:1.1mol:0.55mol=12:22:11,即实验式为C12H22O11,A的摩尔质量为342g/mol,所以分子式也为C12H22O11,故答案为:C12H22O11;
(5)A可发生水解反应,1mol A可水解生成2mol同分异构体,则A为蔗糖,蔗糖水解生成葡萄糖和果糖,其在催化剂作用下水解的化学方程式为C12H22O11(蔗糖)+H2O ![]() C6H12O6(葡萄糖)+C6H12O6(果糖);故答案为:C12H22O11(蔗糖)+H2O
C6H12O6(葡萄糖)+C6H12O6(果糖);故答案为:C12H22O11(蔗糖)+H2O ![]() C6H12O6(葡萄糖)+C6H12O6(果糖)。
C6H12O6(葡萄糖)+C6H12O6(果糖)。

 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案【题目】结合下表回答下列问题(均为常温下的数据):
酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) | 酸 | 电离常数(Ka) |
CH3COOH | 1.8×10-5 | H2CO3 | K1=4.4×10-7 | H2C2O4 | K1=5.4×10-2 | H2S | K1=1.3×10-7 |
HClO | 3×10-8 | K2=4.7×10-11 | K2=5.4×10-5 | K2=7.1×10-15 |
请回答下列问题:
(1) 同浓度的CH3COO-、HCO3-、CO32-、HC2O4-、ClO-、S2-中结合H+的能力最弱的是_________。
(2) 0.1mo1/L的H2C2O4溶液与0.1mo1/L的KOH的溶液等体积混合后所得溶液呈酸性,该溶液中各离子浓度由大到小的顺序为________________。
(3)pH相同的NaC1O和CH3COOK溶液中,[c(Na+)-c(C1O-)]______[c(K+)-c(CH3COO-)](填“>”、“<”或“=”) 。
(4) 向0.1mo1/LCH3COOH 溶液中滴加NaOH 溶液至c(CH3COOH): c(CH3COO-)=5:9,此时溶液pH=_________。
【题目】在一定温度下,将气体X和气体Y各0.16mol充入10 L恒容密闭容器中,发生反应:X(g)+Y(g)![]() 2Z(g) △H<0。反应过程中测定的数据如下表:
2Z(g) △H<0。反应过程中测定的数据如下表:
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
请计算:
(1)反应前2 min的平均速率ν(Z) = __________________________,
(2)到达平衡时,X的转化率为_______________________。