题目内容
13. 铅蓄电池是可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O,下列说法正确的是( )
铅蓄电池是可充电电池,电池总反应式为:Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O,下列说法正确的是( )| A. | 放电时,电解质溶液中H2SO4的浓度将变大 | |
| B. | 放电时,正极反应式为:Pb+SO42--2e-=PbSO4 | |
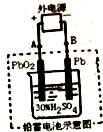
| C. | 放电后用如图所示装置充电,电解质溶液中H+移向左边(PbO2极) | |
| D. | 用如图所示装置充电,阳极反应式为:PbSO4+2H2O-2e-=PbO2+SO42-+4H+ |
分析 A、根据电池的总反应结合硫酸的量的变化情况来回答;
B、放电时,正极发生得电子的还原反应;
C、电解池中,电解质里的阳离子移向阴极,阴离子移向阳极,二次电池充电时,电池的正极和电源的正极相连,电池的负极和电源的负极相连;
D、电解池中,阳极上发生失电子的氧化反应.
解答 解:A、电池总反应式为:Pb+PbO2+4H++2SO42-$?_{充电}^{放电}$2PbSO4+2H2O,放电时,消耗硫酸,电解质溶液中硫酸的浓度将变小,故A错误;
B、放电时,正极发生得电子的还原反应,PbO2中元素化合价降低的是在正极得到电子发生还原反应生成硫酸铅,电极反应为:PbO2+2e-+4H++SO42-=PbSO4+2H2O,故B错误;
C、放电后用如图所示装置充电,电解池中,电解质里的阳离子移向阴极,电池充电时,电池的正极和电源的正极相连,电池的负极和电源的负极相连电解质溶液中氢离子移向左右边(Pb极),故C错误;
D、用如图所示装置充电,阳极上发生失电子的氧化反应,阳极上电极反应式为PbSO4-2e-+2H2O=PbO2+SO42-+4H+,故D正确.
故选D.
点评 本题考查原电池、电解池的工作原理,题目难度中等,本题注意电极反应式的书写及充电时电极的连接规律,为解答该题的关键.

练习册系列答案
相关题目
3.原子序数依次增大的四种短周期元素X、Y、Z、W,其中Y、Z、W同周期,X和W同主族,简单离子半径的大小为X->Y+,其中Z为地壳中含量最高的金属元素,则下列说法正确的是( )
| A. | X和W元素的最高正价相同 | |
| B. | Y、Z均为金属元素,故X、Y、Z三种元素不能形成化合物 | |
| C. | 工业上常利用电解ZW3溶液冶炼金属Z | |
| D. | Y、W的最高价氧化物水化物均能溶解Z单质 |
4.化学与生产、生活密切相关.下列说法不正确的是( )
| A. | 石油裂解可获得乙烯,可从煤干馏得到的煤焦油中提取苯 | |
| B. | 衣服中的棉、麻成分都属于纤维素 | |
| C. | 用纯碱制玻璃,用铁矿石炼铁都会产生温室气体CO2 | |
| D. | 地沟油和矿物油的主要化学成分相同 |
1.下列有关晶体的说法正确的是( )
| A. | 分子晶体中分子间一定存在范德华力 | |
| B. | 晶格能越大,离子晶体的能量越高 | |
| C. | 离子键、共价键、金属键、氢键都是化学键 | |
| D. | 原子间通过共价键形成的晶体一定具有高熔点和高硬度. |
8.下列各组物质属于同系物的是( )
| A. | H2和D2 | B. | 苯和甲苯 | C. | 正丁烷和异丁烷 | D. | 葡萄糖和果糖 |
18.下列金属冶炼的方法错误的是( )
| A. | 加热分解Ag2O冶炼银 | B. | 用CO还原氧化铁冶炼铁 | ||
| C. | 钠与Mg2Cl溶液反应冶炼镁 | D. | 电解熔融氧化铝冶炼铝 |
2.下列说法正确的是( )
| A. | 元素周期表中,电子层数越多,半径一定越大 | |
| B. | 元素周期表中,同一主族,随着核电荷数的递增,熔沸点逐渐降低 | |
| C. | 非金属元素与非金属元素之间可能形成离子键 | |
| D. | 含有离子键的物质一定是离子化合物,只含共价键的物质一定是共价化合物 |
11.现有稀梳酸和稀硝酸的混合溶液,已知稀硝酸浓度2mo/L,取10mL混合酸,加入过量铁粉,生成标准状况下的气体672mL(假设HNO3,只被还原为NO,反应结束后溶液体积不变),则溶液中阳离子浓度为( )
| A. | 3mo/L | B. | 1.5mo/L | C. | 2mo/L | D. | 4mo/L |