题目内容
用石墨电极电解CuCl2溶液(见图)。下列分析正确的是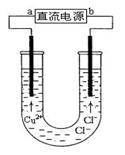
| A.a端是直流电源的负极 |
| B.通电使CuCl2发生电离 |
| C.阳极上发生的反应:Cu2+ + 2e- = Cu |
| D.通电一段时间后,在阴极附近观察到黄绿色气体 |
A
解析试题分析:电解溶液中电源负极连接电解池阴极吸引阳离子,发生还原反应,得到电子,电源正极连接电解池阳极吸引阴离子,发生氧化反应,失去电子。(1)a端吸引溶液中阳离子,即其连接为电解池阴极,a端是电源负极,故A正确;B、溶液中以CuCl2离子状态存在,发生电解反应,故B错误;C、阳极发生失电子的氧化反应,故C错误;D、阴极发生得电子的还原反应Cu2+ + 2e- = Cu,故D错误。
考点:原电池和电解池的工作原理

 53随堂测系列答案
53随堂测系列答案如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和 b 附近分别滴加一滴石蕊溶液。下列实验现象中错误的是
| A.a电极附近呈红色,b电极附近呈蓝色 |
| B.a电极附近呈蓝色,b电极附近呈红色 |
| C.逸出气体的体积,a电极的大于b电极的 |
| D.a、b两电极都逸出无色无味气体 |
镍镉(Ni—Cd)可充电电池在现代生活中有广泛应用。已知某镍镉电池的电解质溶液为KOH溶液,其充、放电按下式进行:Cd+2NiOOH+2H2O Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
Cd(OH)2+2Ni(OH)2。有关该电池的说法正确的是( )
| A.放电时负极附近溶液的pH不变 |
| B.放电时电解质溶液中的OH-向正极移动 |
| C.充电时电池的负极应与电源的负极相连接 |
| D.充电时阳极反应:Ni(OH)2-e-+OH-=NiOOH+H2O |
下列有关金属的说法正确的是( )
| A.不锈钢不易生锈是因为表面有致密保护层 |
| B.纯银的器皿在空气中久置表面变暗是因为发生电化学腐蚀 |
| C.当镀锌铁制品的镀层破损时,镀层还能对铁制品起保护作用 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
如图为某原电池的结构示意图,下列说法正确的是
| A.原电池工作时,电子从铜极流向锌极 |
| B.原电池工作时,铜电极上发生氧化反应 |
| C.正极反应为Zn—2eˉ=Zn2+ |
| D.原电池工作时的总反应为Zn+Cu2+=Zn2++Cu,该反应一定为放热反应 |
最近有研究人员发现了一种处理高浓度乙醛废水的新方法— 隔膜电解法,乙醛分别在阴、阳极发生反应,转化为乙醇和乙酸。实验室以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程,其装置如图所示。下列说法正确的是 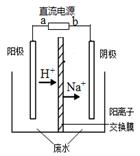
| A.若以CH4—空气燃料电池为直流电源,燃料电池的b极应通入空气 |
| B.电解过程中,阴极区Na2SO4的物质的量增大 |
| C.阳极反应CH3CHO -2e- + 2H+="=" CH3COOH + H2O |
| D.电解过程中,两极除分别生成乙酸和乙醇外,均产生了无色气体,则阳极产生的是O2 |
研究发现,可以用石墨作阳极、钛网作阴极、熔融CaF2—CaO作电解质,利用图示装置获得金属钙,并以钙为还原剂还原二氧化铁制备金属钛。下列说法中正确的是
| A.将熔融CaF2-CaO换成Ca(NO3)2溶液也可以达到相同目的 |
B.阳极的电极反应式为:C+2O2--4e- CO2↑ CO2↑ |
| C.在制备金属钛前后,整套装置中CaO的总量减少 |
| D.若用铅蓄电池作该装置的供电电源,“+"接线柱应连接Pb电极 |
关于铜电极的叙述中不正确的是
| A.铜锌原电池中铜是正极 |
| B.在镀件上镀铜时可用金属铜作阳极 |
| C.用电解法精炼铜时粗铜做阳极 |
| D.用电解法精炼铜时纯铜做阳极 |
以色列科学家达尼埃尔·谢赫特曼因发现“准晶体”获得2011年诺贝尔化学奖。某准晶体由一定比例的铁、铜、铝组成,取两小块该准晶体:一块投入烧杯①中,注入浓氢氧化钠溶液浸没固体;另一块投人烧杯②中,注入稀硫酸浸没固体。下列分析合理的是
| A.在烧杯①中,若构成微型电池,负极反应式为2H2O十2e-=2OH-+H2↑ |
| B.在烧杯②中,若铁、铜构成微型电池,则铜为负极 |
| C.在烧杯①中,若构成微型电池,铝为负极 |
| D.在烧杯②中,向溶液中滴加KSCN溶液,溶液一定变为红色 |