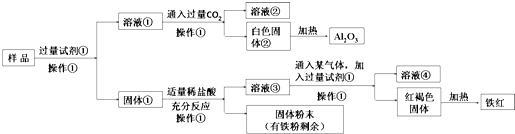
题目内容
9.NaNO2因外观和食盐相似,又有咸味,容易使人误食中毒.已知NaNO2能发生如下反应:2NaNO2+4HI═2NO↑+I2+2NaI+2H2O.(1)上述反应中氧化剂是NaNO2.
(2)根据上述反应,鉴别NaNO2和NaCl.可选用的物质有:①水、②碘化钾淀粉试纸、③淀粉、④白酒、⑤食醋,你认为必须选用的物质有②、⑤(填序号).
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是B(填编号).
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请完成并配平以下化学方程式:□Al+□NaNO3+□NaOH═□NaAlO2+□N2↑+□10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O.若反应过程中转移5mol e-,则生成标准状况下N2的体积为11.2L.
(5)在微生物作用的条件下,NH4+经过两步反应被氧化成NO3ˉ.两步反应的能量变化示意图如图:
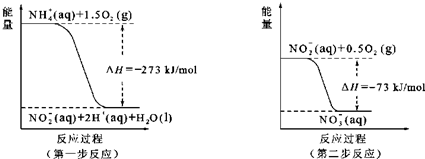
①第一步反应是放热反应(填“放热”或“吸热”),
②1mol NH4+(aq)全部氧化成NO3ˉ(aq)的热化学方程式是:NH4+(aq)+2O2(g)═NO3-(aq)+H2O(l)+2H+(aq)△H=-346kJ•mol-1.
分析 (1)氧化还原反应中,化合价降低元素所在的反应物是氧化剂;
(2)根据反应时有沉淀、气体、颜色变化等明显现象选择试剂;
(3)选择试剂时要考虑:既能使NaNO2转化又无二次污染;
(4)Al元素的化合价由0升高为+3价,N元素的化合价由+5价降低为0,由电子守恒及原子守恒分析;
(5)①第一步反应中,反应物总能量大于生成物总能量;
②1mol NH4+(aq)全部氧化成NO3-(aq)可由两步反应加和得到.
解答 解:(1)2NaNO2+4HI═2NO+I2+2NaI+2H2O,氮元素的化合价降低,所以NaNO2是氧化剂,
故答案为:NaNO2;
(2)①水、③淀粉、④白酒与NaNO2都不反应,所以无明显现象;KI与NaNO2反应生成I2必须在酸性条件下才能反应,食醋会电离出微量的氢离子,碘化钾在食醋本身带的溶剂水中电离出碘离子,亚硝酸钠电离出亚硝酸根与钠离子,发生反应生成碘单质,I2使湿润的淀粉碘化钾试纸变蓝,
故答案为:②⑤;
(3)NaNO2→N2是被还原,必须加还原剂;N元素氧化性弱于O和Cl元素,故只能加NH4Cl作还原剂.方程式为NaNO2+NH4Cl═NaCl+N2↑+2H2O,亚硝酸钠中氮得到3电子指向氮气中的氮,氯化铵中氮失去3电子指向氮气中的氮,
故答案为:B;
(4)Al元素的化合价由0升高为+3价,N元素的化合价由+5价降低为0,该反应还应生成水,由电子守恒及原子守恒可知,反应为10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O,过程中转移5mol e-,则生成标准状况下N2的体积为5mol×$\frac{3}{30}$×22.4L/mol=11.2L,
故答案为:10Al+6NaNO3+4NaOH═10NaAlO2+3N2↑+2H2O;11.2;
(5)①第一步反应中,反应物总能量大于生成物总能量,则该反应为放热反应,△H<0,故答案为:放热;
②1mol NH4+(aq)全部氧化成NO3-(aq)可由两步反应加和得到,热化学方程式为NH4+(aq)+2O2(g)=2H+(aq)+H2O(l)+NO3-(aq)△H=-346kJ/mol,
故答案为:NH4+(aq)+2O2(g)=2H+(aq)+H2O(l)+NO3-(aq)△H=-346kJ/mol.
点评 本题考查较综合,涉及氧化还原反应、配平、热化学反应方程式等,为高频考点,侧重氧化还原反应及能量变化的考查,注意从元素化合价角度及图象角度分析,题目难度不大.

 阅读快车系列答案
阅读快车系列答案| A. | SiO2 CsCl CBr4 CF4 | B. | SiO2 CsCl CF4 CBr4 | ||
| C. | CsCl SiO2 CBr4 CF4 | D. | CF4 CBr4 CsCl SiO2 |
| A. | 阿司匹林 | B. | 氢氧化铝 | C. | 碘酒 | D. | 青霉素 |
| A. | CH3CH2CHO与HCHO | B. |  OH与 OH与 CH2OH CH2OH | ||
| C. | 乙酸与HCOOCH3 | D. | CH3CH2Cl与CH3CH2CH2Br |
| A. | 为了减缓反应速率可用饱和食盐水代替水进行反应 | |
| B. | 该反应为放热反应 | |
| C. | 生成乙炔的反应为CaC2+H2O→CaO+CH≡CH↑ | |
| D. | 为了除去乙炔气体中的杂质可以用CuSO4溶液洗气 |
| A. | 乙烯是石油裂解后的产物 | |
| B. | 芳香烃主要来自于煤的干馏后的煤焦油 | |
| C. | 汽油、煤油、柴油主要来自于石油的常压蒸馏 | |
| D. | 裂化汽油不能使溴水褪色 |
| A. | 0.4 mol O2 | B. | 16g CH4 | ||
| C. | 3.01×1023个H2SO4 | D. | 标准状况下44.8L CO2 |