题目内容
【题目】工业生产中常常需要对混合气体中的NOx含量进行测定,其中一种方法的操作如下:①将200L气样通入酸化的H2O2溶液中,使NOx完全被氧化为NO![]() ,加水稀释至100.00mL;②微微加热,除去过量的H2O2;③量取20.00mL该溶液,加入20mL8.000×10-2mol·L-1FeSO4溶液(过量),充分反应;④用5.000×10-3mol·L-1K2Cr2O7溶液滴定剩余的Fe2+,终点时消耗20.00mL。
,加水稀释至100.00mL;②微微加热,除去过量的H2O2;③量取20.00mL该溶液,加入20mL8.000×10-2mol·L-1FeSO4溶液(过量),充分反应;④用5.000×10-3mol·L-1K2Cr2O7溶液滴定剩余的Fe2+,终点时消耗20.00mL。
(1)能使气样中的NOx更好地被H2O2溶液氧化的操作是___。
(2)NO被H2O2氧化为NO3-的离子方程式是___。
(3)若缺少步骤②,对混合气体中NOx含量的测定结果将___(填“偏大”或“偏小”或“无影响”)。
(4)滴定过程中发生下列反应(未配平):
Fe2++NO![]() +H+——NO↑+Fe3++H2O
+H+——NO↑+Fe3++H2O
Cr2O![]() +Fe2++H+——Cr3++Fe3++H2O
+Fe2++H+——Cr3++Fe3++H2O
则气样中NOx折合成NO2的含量为___mg·m-3。(保留4位有效数字)(写出计算过程)
【答案】将气样缓慢的通过H2O2溶液 2NO+3H2O2=2H++2NO![]() +2H2O 偏大 383.3
+2H2O 偏大 383.3
【解析】
NO被H2O2氧化为NO![]() ,N元素的化合价升高,过氧化氢中O元素的化合价降低;加水稀释硝酸至100.00 mL溶液时,需100mL容量瓶;滴定操作主要用到铁架台、酸式滴定管、锥形瓶等;由反应结合电子守恒可知存在Cr2O72-~6Fe2+~2NO3-,以此计算。
,N元素的化合价升高,过氧化氢中O元素的化合价降低;加水稀释硝酸至100.00 mL溶液时,需100mL容量瓶;滴定操作主要用到铁架台、酸式滴定管、锥形瓶等;由反应结合电子守恒可知存在Cr2O72-~6Fe2+~2NO3-,以此计算。
(1)气体成分中的氮氧化物被H2O2溶液氧化成为NO![]() -进行测定,后续的测定围绕溶液成分展开,气体中的氮氧化物需要被完全吸收测定才更加准确,可以将气样缓慢的通过H2O2溶液,从而增大接触的时间,故答案为:将气样缓慢的通过H2O2溶液;
-进行测定,后续的测定围绕溶液成分展开,气体中的氮氧化物需要被完全吸收测定才更加准确,可以将气样缓慢的通过H2O2溶液,从而增大接触的时间,故答案为:将气样缓慢的通过H2O2溶液;
(2)配平过程中注意溶液是酸性环境,用H+配平,离子方程式为:2NO+3H2O2=2H++2NO![]() +2H2O,故答案为:2NO+3H2O2=2H++2NO
+2H2O,故答案为:2NO+3H2O2=2H++2NO![]() +2H2O;
+2H2O;
(3)若缺少步骤②,过量的H2O2就没有除去,当加入FeSO4标准溶液时,过量的H2O2也氧化了一部分Fe2+,使加入的K2Cr2O7标准溶液偏少,测定结果偏大,故答案为:偏大;
(4)计算过程如下:
实验过程中消耗的n(Cr2O72-)=5.000×10-3mol/L×20.00mL×10-3L/mL=1.000×10-4mol,由滴定时的反应Cr2O72-+6Fe2++14H+=6Fe3++2Cr3++7H2O,则n(Fe2+)=6n(Cr2O72-)=6×1.000×10-4mol=6.000×10-4mol,与NO3-反应的Fe2+的物质的量:n(Fe2+)=8.000×10-2mol/L×20.00mL×10-3L/mL-6.000×10-4mol=1.000×10-3mol,气样中NOx的物质的量:n(NOx)=n(NO2)=n(NO3–)=![]() ,气样中NOx折合成NO2的质量=m(NO2)=
,气样中NOx折合成NO2的质量=m(NO2)=![]() =76.66mg,气样中NOx折合成NO2的含量=
=76.66mg,气样中NOx折合成NO2的含量=![]() =383.3mg·m-3,故答案为:383.3。
=383.3mg·m-3,故答案为:383.3。

 阅读快车系列答案
阅读快车系列答案【题目】某同学设计如下三个实验方案以探究某反应是放热反应还是吸热反应:
方案一:如图1,在小烧杯里放一些除去氧化铝保护膜的铝片,然后向烧杯里加入10 mL 2 mol·L-1稀硫酸,再插入一支温度计,温度计的温度由20 ℃逐渐升至75 ℃,随后,温度逐渐下降至30 ℃,最终停留在20 ℃。
方案二:如图2,在烧杯底部用熔融的蜡烛粘一块小木片,在烧杯里加入10 mL 2 mol·L-1硫酸溶液,再向其中加
入氢氧化钠溶液,片刻后提起烧杯,发现小木片脱落下来。
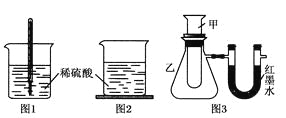
方案三:如图3,甲试管中发生某化学反应,实验前U形管红墨水液面相平,在化学反应过程中,通过U形管两侧红
墨水液面高低判断某反应是吸热反应还是放热反应。
序号 | 甲试管里发生反应的物质 | U形管里红墨水液面 |
① | 氧化钙与水 | 左低右高 |
② | 氢氧化钡晶体与氯化铵晶体(充分搅拌) | ? |
③ | 铝片与烧碱溶液 | 左低右高 |
④ | 铜与浓硝酸 | 左低右高 |
根据上述实验回答相关问题:
(1)铝片与稀硫酸的反应是________(填“吸热”或“放热”)反应,写 出该反应的离子方程式:___________。
(2)方案一中,温度升至最大值后又下降的原因是___________。
(3)方案二中,小木片脱落的原因是________,由此得出的结论是__________________。
(4)方案三中,如果甲试管里发生的反应是放热反应,则U形管里红墨水液面:左边________(填“高于”“低于”或“等于”)右边。
(5)由方案三的现象得出结论:①③④组物质发生的反应都是________(填“吸热”或“放热”)反应,如果放置较长时间,可观察到U形管里的现象是______________。
(6)方案三实验②的U形管中的现象为________,说明反应物的总能量________(填“大于”“小于”或“等于”)生成物的总能量
【题目】在温度、容积相同的3个密闭容器中,按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时的有关数据如下[已知N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1],下列说法正确的是( )
2NH3(g) ΔH=-92.4 kJ·mol-1],下列说法正确的是( )
容器 | 甲 | 乙 | 丙 |
反应物投入量 | 1 mol N2、 3 mol H2 | 2 mol NH3 | 4 mol NH3 |
NH3的浓 度/mol·L-1 | c1 | c2 | c3 |
反应的能量变化 | 放出a kJ | 吸收b kJ | 吸收c kJ |
体系压强(Pa) | p1 | p2 | p3 |
反应物转化率 | α1 | α2 | α3 |
A. 2c1>c3B. α1+α3<1C. 2p2<p3D. a+b>92.4