题目内容
下列说法正确的是
| A.pH=2的溶液中的c(H+)是pH=4的溶液中的c(H+)的2倍 |
| B.等浓度的Na2CO3溶液的pH大于NaHCO3溶液的pH |
| C.25℃时纯水的pH低于100℃时纯水的pH |
| D.pH=3的硫酸溶液中的c(H+)是pH=3的盐酸溶液中c(H+)的2倍 |
B
A错,pH=2的溶液中的c(H+)是pH=4的溶液中的c(H+)的100倍;B正确;C错,25℃时纯水的pH大于100℃时纯水的pH;D错,.pH=3的硫酸溶液中的c(H+)与pH=3的盐酸溶液中c(H+)相等;

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
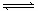 H++OH— △H>0,下列叙述正确的是( )
H++OH— △H>0,下列叙述正确的是( ) ________25 ℃。
________25 ℃。