题目内容
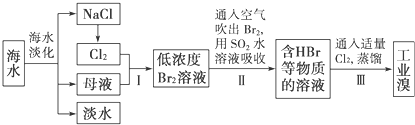
15.海水是巨大的资源宝库,在海水淡化及综合利用方面天津市位居全国前列.从海水中提取食盐和溴的过程如下:已知:①海水中溴元素的浓度0.067g/L;
②Br2的沸点为59℃,微溶于水,有毒性和强腐蚀性.
(1)请写出一种海水淡化的方法:蒸馏法(或电渗析法、离子交换法).
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为富集溴元素.
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为SO2+Br2+2H2O=4H++SO42-+2Br-.
(4)某化学研究性学习小组为了从工业溴中提纯溴的方法,绘制了如下装置简图:

请你参与分析讨论:
①图中仪器B的名称:冷凝管.
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因为Br2腐蚀橡胶.
③实验中要达到提纯溴的目的,操作的关键是控制温度计b的温度,并收集沸点为59℃时的馏分.
④C中液体产物颜色为深红棕色,为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是分液(或蒸馏).
分析 通过海水蒸发得到淡水、NaCl、母液,向母液中通入氯气,发生反应Cl2+2Br-=2Cl-+Br2,利用热空气吹出溴,用SO2吸收Br2,发生反应SO2+Br2+2H2O=H2SO4+2HBr,向溶液中通入氯气发生反应Cl2+2Br-=2Cl-+Br2,然后采用萃取的方法获取Br2,以此解答该题.
解答 解:通过海水蒸发得到淡水、NaCl、母液,向母液中通入氯气,发生反应Cl2+2Br-=2Cl-+Br2,利用热空气吹出溴,用SO2吸收Br2,发生反应SO2+Br2+2H2O=H2SO4+2HBr,向溶液中通入氯气发生反应Cl2+2Br-=2Cl-+Br2,然后采用萃取的方法获取Br2.
(1)海水淡化的有蒸馏法、电渗析法、离子交换法等,故答案为:蒸馏法(或电渗析法、离子交换法);
(2)海水中溴元素含量较少,步骤I中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为富集溴元素,故答案为:富集溴元素;
(3)在水溶液里溴和二氧化硫反应离子方程式为SO2+Br2+2H2O=4H++SO42-+2Br-,
故答案为:SO2+Br2+2H2O=4H++SO42-+2Br-;
(4)①图中仪器B的名称是冷凝管,故答案为:冷凝管;
②溴能腐蚀橡胶,所以整套实验装置中仪器连接均不能用橡胶塞和橡胶管,故答案为:Br2腐蚀橡胶;
③Br2的沸点为59℃,蒸馏水应控制蒸馏烧瓶内的温度计温度,a为水浴加热温度,故答案为:b;59℃;
④C中液体产物为溴,颜色为深红棕色,为除去该产物中仍残留的少量C12,可向其中加入NaBr溶液,充分反应后,再进行分离的操作是分液,
故答案为:深红棕色;分液(或蒸馏).
点评 本题考查物质的分离、提纯的综合应用,侧重于海水资源的综合利用的考查,从整体上把握溴的提纯过程,知道提纯过程中发生的反应及基本操作方法,再结合物质的性质分析解答,题目难度不大.

| B12结构单元 | SF6分子 | S8分子 | HCN | |
| 结 构 模 型 示 意 图 |  |  |  |  |
| 备注 | 熔点1873K | 易溶于CS2 |
| A. | 单质硼属于原子晶体,结构单元中含有30个B-B键,含有20个正三角形 | |
| B. | SF6是由极性键构成的非极性分子 | |
| C. | 固态硫S8属于原子晶体 | |
| D. | HCN的结构式为H-C≡N |
| A. | 配制一定物质的量浓度溶液的实验中,不需要精确量取水的用量 | |
| B. | 溶液注入容量瓶前不需要恢复到室温 | |
| C. | 用胶头滴管定容后需反复倒转摇匀,若发现液面低于刻度线时要小心地加些水 | |
| D. | 若加水定容时超过了刻度线,赶快用胶头滴管吸走超出的部分 |
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡 常数(25℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | 2CN-+H2O+CO2═2HCN+CO32- | |
| B. | 2HCOOH+CO32-═2HCOO-+H2O+CO2↑ | |
| C. | 等浓度的HCOONa和NaCN溶液的pH前者大于后者 | |
| D. | 中和等浓度的HCOOH和HCN消耗NaOH的量前者等于后者 |
| A. | 33.3% | B. | 25.0% | C. | 50.0% | D. | 53.3% |
| A. |  | B. | 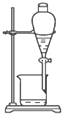 | ||
| C. | 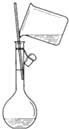 | D. |  |
| A. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| C. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| D. | 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |