题目内容
【题目】A、B、C、D四种短周期元素,原子序数D>C>B>A,且B、C、D同周期,A、D同主族,B原子的最外层只有一个电子,C的原子结构示意图如图,D在同周期元素中原子半径最小,据此填空:

(1)C元素的名称为____,其气态氢化物的化学式为___。
(2)D在周期表的___周期,___族。
(3)A、B、C、D四种元素的原子半径由大到小的顺序为(用化学式填写)___
(4)B的最高价氧化物的水化物的化学式为__
【答案】硅 SiH4 三 VIIA Na Si Cl F NaOH
【解析】
A. B. C.D四种短周期元素,原子序数D>C>B>A,C的原子结构示意图为 ,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、 C、D同周期,且B原子的最外层只有一个电子,故B为Na。
,第一电子层只能容纳2个电子,故x=2,则C原子核外电子数为14,C为Si元素;D在同周期元素中原子半径最小,处于ⅦA族,原子序数大于Si,故D为Cl;A、D同主族,则A为F元素;B、 C、D同周期,且B原子的最外层只有一个电子,故B为Na。
(1)C元素的名称为硅,其气态氢化物的化学式为SiH4,故答案为:硅;SiH4;
(2)D为Cl元素,处于在周期表中第三周期ⅦA族,故答案为:三;ⅦA;
(3)同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径Na>Si>Cl>F,故答案为:Na>Si>Cl>F;
(4)Na的最高价氧化物的水化物的化学式为NaOH,故答案为:NaOH.

【题目】如图所示,某化学兴趣小组设计了一个燃料电池,并探究氯碱工业原理和粗铜精炼原理,其中乙装置中X为阳离子交换膜。根据要求回答相关问题:
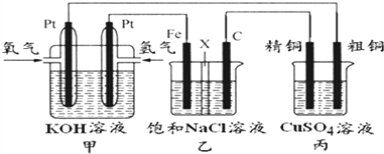
(1)通入氧气的电极为_____(填“正极”或“负极”),通氢气一极的电极反应式为_________________;
(2)铁电极为_______(填“阳极”或“阴极”),乙装置中电解反应的化学方程式为_________________。
(3)若在标准状况下,有1.12 L氧气参加反应,丙装置中阴极增重的质量为______g;
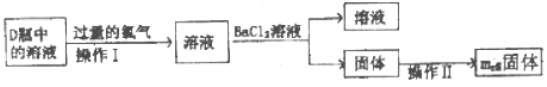
(4)某粗铜中含有铁、金、银和铂等杂质,通过电解精制后,为从电解液中制得硫酸铜晶体(CuSO4·5H2O),设计了如下工艺流程:
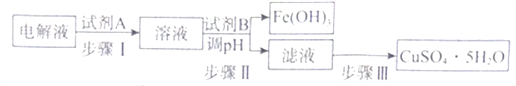
已知:几种金属阳离子开始沉淀和沉淀完全的pH:
氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
Fe3+ | 1.9 | 3.2 |
Fe2+ | 7.0 | 9.0 |
Cu2+ | 4.7 | 6.7 |
①步骤I中加入试剂A的目的是_____________________________,试剂A应选择______(填序号);
a.氯气 b.过氧化氢 C.酸性高锰酸钾溶液
选择该试剂的原因_____________________________________________________;
②步骤II中试剂B为_________,调节pH的范围是___________;
③步骤III的操作是加热浓缩、_______、___________。