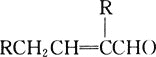题目内容
【题目】某研究性学习小组为合成1-丁醇,查阅资料得知下列合成路线:CH3CH=CH2+CO+H2![]() CH3CH2CH2CHO
CH3CH2CH2CHO ![]() CH3CH2CH2OH;CO的制备原理:HCOOH
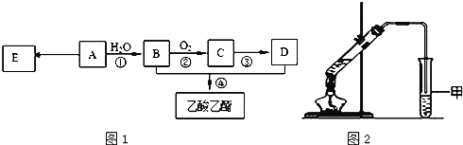
CH3CH2CH2OH;CO的制备原理:HCOOH![]() CO↑+H2O,并设计出原料气的制备装置如图所示。
CO↑+H2O,并设计出原料气的制备装置如图所示。
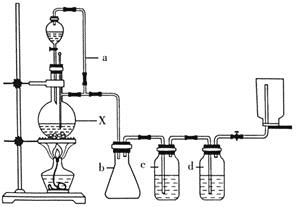
请填写下列空白:
(1)若用以上装置制备干燥纯净的CO,仪器X的名称是________;装置中b的作用是________;c和d中盛装的试剂分别是________,________。
(2)实验室现有浓硫酸、2-丙醇,请写出制备丙烯的化学方程式:________________________。
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,该小组用以下试剂检验这四种气体,混合气体通过试剂的顺序是________(填序号)。
①饱和Na2SO3溶液 ②酸性KMnO4溶液 ③石灰水 ④无水CuSO4 ⑤品红溶液
(4)正丁醛经催化剂加氢得到含少量正丁醛的1-丁醇粗品,为纯化1-丁醇,该小组查阅文献得知:①R-CHO+NaHSO3(饱和)→RCH(OH)SO3Na↓;②沸点:乙醚34℃,1-丁醇118℃,并设计出如下提纯路线:

试剂1为________,操作2为________,操作3为________。
【答案】蒸馏烧瓶 防倒吸 NaOH溶液 浓![]() (CH3)2CHOH
(CH3)2CHOH![]() CH2=CHCH3↑+H2O
CH2=CHCH3↑+H2O ![]() 或
或![]() 饱和
饱和![]() 溶液 萃取 蒸馏
溶液 萃取 蒸馏
【解析】
(1)根据装置图判断仪器X的名称;b为安全瓶,可防止倒吸;c和d可分别除去挥发出的HCOOH和水蒸气,由此选择盛装的试剂;
(2)2-丙醇发生分子内脱水,生成丙烯和水,由此书写方程式;
(3)制丙烯时,还产生少量SO2、CO2及水蒸气,可先除去水蒸气,再检验是否存在SO2,并用饱和Na2SO3溶液和酸性KMnO4溶液除去SO2,最后检验CO2和丙烯,由此确定试剂的顺序;
(4)根据流程可知,粗产品中含有正丁醛,利用反应①可知饱和亚硫酸氢钠溶液可与正丁醛发生反应生成沉淀,通过过滤可除去沉淀;加入乙醚可萃取溶液中的1-丁醇,1-丁醇和乙醚的沸点相差较大,可利用蒸馏的方法分离,由此作答。
(1)仪器X的名称是蒸馏烧瓶,甲酸在浓硫酸的作用下通过加热脱水即生成CO,由于甲酸易挥发,产生的CO中必然会混有甲酸,所以在收集之前需要除去甲酸,可以利用NaOH溶液吸收甲酸;又因为甲酸易溶于水,所以必需防止液体倒流,即b的作用是防止倒吸,最后通过浓硫酸干燥CO;
(2)2-丙醇发生分子内脱水可制丙烯,方程式为(CH3)2CHOH![]() CH2=CHCH3↑+H2O;
CH2=CHCH3↑+H2O;
(3)检验丙烯可用酸性KMnO4溶液,检验SO2可用酸性KMnO4溶液褪色、品红溶液或石灰水,检验CO2可用石灰水,检验水蒸气可用无水CuSO4,所以在检验这四种气体必需考虑试剂的选择和顺序,只要通过溶液,就会产生水蒸气,因此先检验水蒸气;然后检验SO2并在检验之后除去SO2,除SO2可以用饱和Na2SO3溶液,最后检验CO2和丙烯,因此顺序为④⑤①②③或④⑤①③②;
(4)粗品中含有正丁醛,根据所给的信息利用饱和NaHSO3溶液形成沉淀,然后通过过滤即可除去;由于饱和NaHSO3溶液是过量的,所以加入乙醚的目的是萃取溶液中的1-丁醇,因为1-丁醇和乙醚的沸点相差很大,因此可以利用蒸馏将其分离开,因此试剂1为饱和NaHSO3溶液,操作2为萃取,操作3为蒸馏。

 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案【题目】丙烯酸是合成丙烯酸脂的原料,丙烯醇用于生产甘油、塑料等。某小组以丙烯醛为原料生产丙烯醇、丙烯酸的流程如图所示:
 已知反应原理:
已知反应原理:![]()
![]()
有关物质的物理性质如表:
| 丙烯醛 | 丙烯醇 | 丙烯酸 | 四氯化碳 |
沸点/℃ | 53 | 97 | 141 | 77 |
熔点/℃ | -87 | -129 | 13 | -22.8 |
密度/gcm-3 | 0.84 | 0.85 | 1.02 | 1.58 |
溶解性(常温) | 易溶于水和 有机物 | 溶于水和 有机溶剂 | 溶于水和 有机溶剂 | 难溶于水, 易溶于有机物 |
(1)已知苯的沸点为80.1℃,上述步骤②的萃取剂用四氯化碳而不用苯,其主要原因可能是_________________。上层液体分液漏斗________(填“上”或“下”)口倒(或放)出。
(2)从步骤④的残留液中可提取一种无水正盐,它是________(填化学式)。
(3)步骤⑤采用如图装置,该装置有一处明显错误,请指出错误:________,并改之。收集丙烯醇的温度应控制在________左右。

(4)已知:醛类具有较强还原性,能与溴水、酸性高锰酸钾溶液、银氨溶液等反应。某同学为了证明丙烯酸产品中含有丙烯醛,设计如下方案:
a.取少量溴水于试管,加入适量丙烯酸样品,振荡,溶液褪色
b.取少量酸性高锰酸钾溶液于试管,加入适量丙烯酸样品,振荡,溶液褪色
c.取少量银氨溶液于试管,加入适量丙烯酸样品,用水浴加热,有银镜产生
d.取少量酸性重铬酸钾溶液于试管,加入适量丙烯酸样品,振荡,溶液由橙红色变成绿色
上述方案中,能证明丙烯酸产品中含少量丙烯醛的是________(填字母)。
(6)为了证明丙烯酸是弱酸,设计如下方案,其中能达到实验目的的是________(填字母)。
代号 | 方案 | 预测现象 |
A | 取少量 | 溶液变红色 |
B | 常温下,将10ml0.1molL-1NaOH溶液和10ml0.1molL-1 | pH>7 |
C | 用相同的导电仪分别测定盐酸溶液、 | 前者灯泡较亮 |
【题目】硼镁泥是硼镁矿生产硼砂晶体![]() 时的废渣,其主要成分是MgO,还含有
时的废渣,其主要成分是MgO,还含有![]() 、CaO、
、CaO、![]() 、FeO、MnO、
、FeO、MnO、![]() 等杂质。以硼镁泥为原料制取七水硫酸镁的工艺流程如下:
等杂质。以硼镁泥为原料制取七水硫酸镁的工艺流程如下:
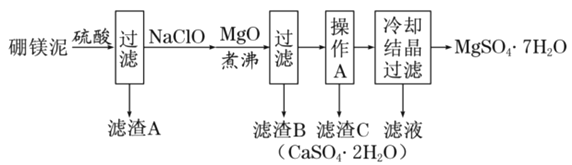
回答下列问题:
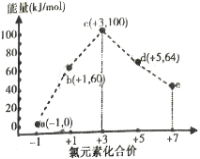
(1)![]() 中B的化合价为__________。
中B的化合价为__________。
(2)![]() 易溶于水,也易发生水解:
易溶于水,也易发生水解:![]() 硼酸
硼酸![]() 硼酸在常温下溶解度较小
硼酸在常温下溶解度较小![]() 。写出加入硫酸时
。写出加入硫酸时![]() 发生反应的化学方程式:_____。
发生反应的化学方程式:_____。
(3)滤渣B中含有不溶于稀盐酸但能溶于热浓盐酸的黑色固体,写出生成黑色固体的离子方程式____________。
(4)加入MgO的目的是___________________。
(5)已知![]() 、
、![]() 的溶解度如下表:
的溶解度如下表:
温度 | 40 | 50 | 60 | 70 |
|
|
|
|
|
|
|
|
|
|
“操作A”是将![]() 和
和![]() 混合溶液中的
混合溶液中的![]() 除去,根据上表数据,简要说明“操作A”步骤为____________________。
除去,根据上表数据,简要说明“操作A”步骤为____________________。
(6)硼砂也能在工业上制取![]() ,
,![]() 被称为有机化学中的“万能还原剂”。
被称为有机化学中的“万能还原剂”。
![]() 写出
写出![]() 的电子式:___________。
的电子式:___________。
![]() “有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克
“有效氢含量”可用来衡量含氢还原剂的还原能力,其定义是:每克含氢还原剂的还原能力相当于多少克![]() 的还原能力。
的还原能力。![]() 的有效氢含量为_________
的有效氢含量为_________![]() 保留两位小数
保留两位小数![]() 。
。
![]() 在碱性条件下,在阴极上电解
在碱性条件下,在阴极上电解![]() 也可制得硼氢化钠,写出阴极室的电极反应式:________。
也可制得硼氢化钠,写出阴极室的电极反应式:________。