题目内容
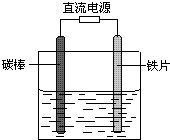 如图所示,电解未精制饱和食盐水(含有少量Mg2+),在碳棒和铁片表面均有气体生成,一段时间后铁片附近出现浑浊现象.下列叙述正确的是( )
如图所示,电解未精制饱和食盐水(含有少量Mg2+),在碳棒和铁片表面均有气体生成,一段时间后铁片附近出现浑浊现象.下列叙述正确的是( )| A、碳棒接直流电源的负极 |
| B、碳棒上发生还原反应 |
| C、铁片上的电极反应式为2Cl--2e-═Cl2↑ |
| D、铁片附近出现的浑浊物是Mg(OH)2 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:在碳棒和铁片表面均有气体生成,一段时间后铁片附近出现浑浊现象,可知碳为阳极,Fe为阴极,电解饱和食盐水,阳极上阴离子放电,阴极上阳离子放电,同时阴极生成氢氧化镁沉淀,以此解答该题.
解答:
解;A.碳棒为阳极,连接电源的正极,故A错误;
B.碳棒为阳极,发生氧化反应,故B错误;
C.铁片为阴极,发生还原反应,电极方程式为2H++2e-=H2↑,故C错误;
D.阴极发生2H++2e-=H2↑,同时生成OH-,则出现的浑浊物是Mg(OH)2,故D正确.
故选D.
B.碳棒为阳极,发生氧化反应,故B错误;
C.铁片为阴极,发生还原反应,电极方程式为2H++2e-=H2↑,故C错误;
D.阴极发生2H++2e-=H2↑,同时生成OH-,则出现的浑浊物是Mg(OH)2,故D正确.
故选D.
点评:本题考查电解食盐水,为高频考点,侧重于学生的分析能力的考擦哈,明确电解原理、离子的放电顺序,发生的电极反应即可解答,题目较简单.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列叙述不正确的是( )
| A、NH3易液化,液氨常用做制冷剂 |
| B、与金属反应时,稀HNO3可能被还原为更低价态,则稀硝酸氧化性强于浓硝酸 |
| C、氨盐受热易分解,因此贮存氨态氮肥时要密封保存,并放在阴凉通风处 |
| D、活泼金属不能从稀硝酸中置换出氢气 |
下列关于金属腐蚀的说法不正确的是( )
A、金属吸氧腐蚀的实质是:M+nH2O═M(OH)n+
| ||
| B、金属的化学腐蚀的实质是M-ne-═Mn+,电子直接转移给氧化剂 | ||
| C、金属的化学腐蚀不一定在酸性条件下进行 | ||
| D、在潮湿的中性环境中,金属的电化学腐蚀主要是吸氧腐蚀 |
下列与化学反应能量变化相关的叙述正确的是( )
| A、生成物总能量一定低于反应物总能量 |
| B、放热反应的反应速率总是大于吸热反应的反应速率 |
| C、任何化学反应必然伴随着能量的变化 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件下的△H不同 |
在一定温度下,向一个容积为2L的密闭容器内(预先加入催化剂)通入2mol NH3,经过一段时间后,测得容器内的压强为起始时的1.2倍.则NH3的转化率为( )
| A、25% | B、80% |
| C、10% | D、20% |
下列有机物的命名正确的是( )
A、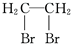 二溴乙烷 二溴乙烷 |
B、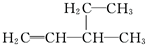 3乙基1丁烯 3乙基1丁烯 |
C、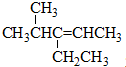 3乙基4甲基-2-戊烯 3乙基4甲基-2-戊烯 |
D、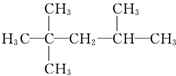 2,2,4三甲基戊烷 2,2,4三甲基戊烷 |
在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ?mol-1
由1mol CO和3mol CH4组成的混合气体在上述条件下完全燃烧时,释放的热量为( )
2CO(g)+O2(g)═2CO2(g)△H=-566kJ?mol-1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=-890kJ?mol-1
由1mol CO和3mol CH4组成的混合气体在上述条件下完全燃烧时,释放的热量为( )
| A、2 912 kJ |
| B、2 953 kJ |
| C、3 236 kJ |
| D、3 867 kJ |
固体A的化学式为NH5,能跟水反应,它的所有原子的电子层结构都跟与该原子同周期的稀有气体原子一样,则下列说法中,不正确的是( )
| A、1mol NH5中有5NA个N-H键(NA为阿伏加德罗常数) |
| B、NH5中既有共价键、又有离子键,是离子晶体 |
| C、NH5跟水的反应是氧化还原反应 |
| D、NH5跟水反应的化学方程式为:NH5+H2O═NH3?H2O+H2↑ |
化学学习中,推理是一种重要的学习方法,下列推论正确的是( )
| A、由“BF3和SO3互为等电子体”,可推知二者均为非极性分子 |
| B、由“某过程发生化学键断裂”,可推知该过程发生了化学变化 |
| C、由“蒸干NaCl溶液得NaCl固体”,可推知蒸干MgCl2溶液得MgCl2固体 |
| D、由“同温度下等浓度的Na2CO3溶液比Na2SO3溶液的pH大”,可推知C比S的非金属性弱 |