题目内容
【题目】如图中分别是某课外活动小组设计的制取氨气并用氨气进行喷泉实验的两组装置,回答下列问题:
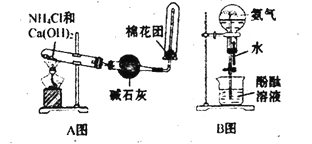
(1)用A图所示的装置可制备干燥的NH3,反应的化学方程式为:___。干燥管中干燥剂能否改用无水CaCl2?__。(填“能”或“不能”)检验NH3是否收集满的实验方法是:__。氨气溶于水呈碱性的原因是:___。
(2)若要配制100mL9.0mol/L的氨水,用到的玻璃仪器有烧杯、玻璃棒、量筒、___、__。
(3)将等浓度、等体积的氨水和盐酸混合,所得溶液中离子浓度从大到小的顺序为___。
(4)用B图所示的装置可进行喷泉实验,上部烧瓶已充满干燥氨气,引发水上喷的操作是__,该实验的原理是:___。
【答案】2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 不能 用湿润的红色石蕊试纸靠近集气瓶口附近,若试纸变蓝;则说明NH3已收集满(或用玻璃棒蘸取少许浓盐酸靠近收集NH3的试管口,若产生白烟,说明试管已收集满NH3,反之,则没有收集满) 由于NH3+H2O
CaCl2+2NH3↑+2H2O 不能 用湿润的红色石蕊试纸靠近集气瓶口附近,若试纸变蓝;则说明NH3已收集满(或用玻璃棒蘸取少许浓盐酸靠近收集NH3的试管口,若产生白烟,说明试管已收集满NH3,反之,则没有收集满) 由于NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,故溶液呈弱碱性 100mL容量瓶 胶头滴管 c(Cl-)>c(NH4+)>c(H+)>c(OH-) 挤压胶头滴管橡胶乳头,使少量水进入烧瓶,并及时打开止水夹 NH3极易溶于水,致使烧瓶内压强迅速减小
NH4++OH-,故溶液呈弱碱性 100mL容量瓶 胶头滴管 c(Cl-)>c(NH4+)>c(H+)>c(OH-) 挤压胶头滴管橡胶乳头,使少量水进入烧瓶,并及时打开止水夹 NH3极易溶于水,致使烧瓶内压强迅速减小
【解析】
(1)①实验室用氯化铵和氢氧化钙加热制取氨气;无水氯化钙和氨气能发生反应生成络合物;根据氨气的性质和氨水的性质分析解答;
(2)若要配制100mL9.0mol/L的氨水,需要选用100mL容量瓶配制,结合实验步骤分析需要的玻璃仪器;
(3)将等浓度、等体积的氨水和盐酸混合,恰好反应生成氯化铵溶液,氯化铵属于强酸弱碱盐,铵根离子水解,溶液显酸性,据此分析排序;
(4)NH3极易溶于水,氨气溶于水后,能够使烧瓶内压强迅速减小,据此分析解答。
(1)①在加热条件下,氯化铵和氢氧化钙反应生成氯化钙、水和氨气,反应的化学方程式为2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;无水氯化钙和氨气能发生反应CaCl2+8NH3=CaCl28NH3,所以干燥管中干燥剂不能改用无水CaCl2;氨气的水溶液显碱性,NH3+H2O
CaCl2+2NH3↑+2H2O;无水氯化钙和氨气能发生反应CaCl2+8NH3=CaCl28NH3,所以干燥管中干燥剂不能改用无水CaCl2;氨气的水溶液显碱性,NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,可以用湿润的红色石蕊试纸靠近集气瓶口附近,若试纸变蓝;则说明NH3已收集满,故答案为:2NH4Cl+Ca(OH)2
NH4++OH-,可以用湿润的红色石蕊试纸靠近集气瓶口附近,若试纸变蓝;则说明NH3已收集满,故答案为:2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O;不能;用湿润的红色石蕊试纸靠近集气瓶口附近,若试纸变蓝;则说明NH3已收集满(或用玻璃棒蘸取少许浓盐酸靠近收集NH3的试管口,若产生白烟,说明试管已收集满NH3,反之,则没有收集满);由于NH3+H2O
CaCl2+2NH3↑+2H2O;不能;用湿润的红色石蕊试纸靠近集气瓶口附近,若试纸变蓝;则说明NH3已收集满(或用玻璃棒蘸取少许浓盐酸靠近收集NH3的试管口,若产生白烟,说明试管已收集满NH3,反之,则没有收集满);由于NH3+H2O![]() NH3·H2O
NH3·H2O![]() NH4++OH-,故溶液呈弱碱性;
NH4++OH-,故溶液呈弱碱性;
(2)若要配制100mL9.0mol/L的氨水,需要选用100mL容量瓶配制,配制过程中用到的玻璃仪器有烧杯、玻璃棒、量筒、胶头滴管,故答案为:100mL容量瓶;胶头滴管;
(3)将等浓度、等体积的氨水和盐酸混合,恰好反应生成氯化铵溶液,氯化铵属于强酸弱碱盐,铵根离子水解,溶液显酸性,所得溶液中离子浓度从大到小的顺序为c(Cl-)>c(NH4+)>c(H+)>c(OH-),故答案为:c(Cl-)>c(NH4+)>c(H+)>c(OH-);
(4)NH3极易溶于水,氨气溶于水后,能够使烧瓶内压强迅速减小,引发喷泉,用氨气进行喷泉实验时,引发水上喷的操作是挤压胶头滴管橡胶乳头,使少量水进入烧瓶,并及时打开止水夹,故答案为:挤压胶头滴管橡胶乳头,使少量水进入烧瓶,并及时打开止水夹;NH3极易溶于水,致使烧瓶内压强迅速减小。

 阅读快车系列答案
阅读快车系列答案