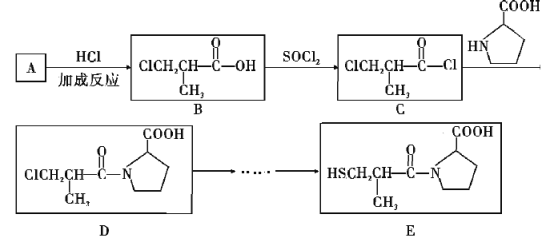
题目内容
【题目】日前新合成的砷化镉三维材料具有超强导电性,这种材料的电气性能与石墨烯相当,可代替石墨烯使用。
(1)Cd与Zn同族且相邻,若Cd基态原子将次外层1个d电子激发进入最外层的np能级,则该激发态原子的外围电子排布式为___。
(2)与砷(As)同主族的N、P两种元素的氢化物水溶液的碱性:NH3强于PH3,分析其原因是___。
(3)As、Ge、Se的第一电离能由大到小的顺序为___(用元素符号表示)。
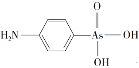
(4)含砷有机物“对氨基苯胂酸”的结构简式如图,其中C原子轨道杂化类型为___,1mol对氨基苯胂酸含σ键数目为___。
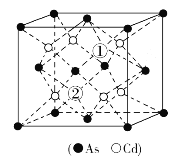
(5)砷化镉可以看作是石墨烯的3D版,其晶胞结构如图,As为面心立方堆积,Cd占据As围成的四面体空隙,空隙占有率75%,如图“①”和“②”位是“空位”。则砷化镉化学式为___。
【答案】4d95s25p1 原子半径N<P,电负性N>P,NH3更易结合水电离的H+ As>Se>Ge sp2 19NA(或19×6.02×1023) Cd3As2
【解析】
(1)Cd与Zn同族且相邻,则基态Cd原子的外围电子排布与Zn类似,为4d105s2,受到激发后次外层1个d电子即4d能级上的一个电子,激发进入最外层的5p能级,所以激发态Cd外围电子排布为4d95s25p1;
(2)原子半径N<P,电负性N>P,NH3更易结合水电离的H+,所以氢化物水溶液的碱性:NH3强于PH3;
(3)Ge、As、Se为同周期主族元素,且原子序数依次增大,同周期主族元素自左至右第一电离能呈增大趋势,但As为第ⅤA族元素,其4p能级为半满状态,更稳定,第一电离能大于相邻元素,所以第一电离能As>Se>Ge;
(4)苯环中含有大π键,环上的C原子为sp2杂化;苯环上有6个碳原子之间形成的σ键,还有4个碳氢原子之间形成的σ键,砷氧双键中有一个σ键,其余单键均为σ键,所以1mol对氨基苯胂酸含σ键数目为19NA(或19×6.02×1023);
(5)根据晶胞结构,晶胞中 As原子的个数为![]() =4,Cd原子的个数为6,所以砷化镉的化学式为Cd3As2。
=4,Cd原子的个数为6,所以砷化镉的化学式为Cd3As2。

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案