题目内容
10.下列各组中的性质比较中,正确的有( )| A. | 酸性 HClO4>HBrO4>HIO4 | B. | 碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2 | ||
| C. | 非金属性 F>Cl>Br | D. | 稳定性 HCl>H2S>PH3 |
分析 A.同主族元素从上到下元素的非金属性逐渐减弱,对应的最高价氧化物的水化物的酸性逐渐减弱;
B.同主族元素的金属性从上到下逐渐增强,对应的最高价氧化物的水化物的进行逐渐正确;
C.同主族元素从上到下元素的非金属性逐渐减弱;
D.同周期元素从左到右非金属性逐渐增强,其氢化物的稳定性增强.
解答 解:A.Cl、Br、I位于同一主族,同主族元素从上到下元素的非金属性逐渐减弱,对应的最高价氧化物的水化物的酸性逐渐减弱,故A正确;
B.同主族元素的金属性从上到下逐渐增强,对应的最高价氧化物的水化物的进行逐渐增强,则碱性 Ba(OH)2>Ca(OH)2>Mg(OH)2,故B正确;
C.同主族元素从上到下元素的非金属性逐渐减弱,则非金属性 F>Cl>Br,故C正确;
D.同周期元素从左到右非金属性逐渐增强,其氢化物的稳定性增强,则稳定性 HCl>H2S>PH3,故D正确.
故答案为:ABCD.
点评 本题考查元素周期表的递变规律,题目难度不大,注意单质、化合物的性质与金属性、非金属性的关系.

练习册系列答案
相关题目
18. 研究氮机器化合物对化工生产有重要意义.
研究氮机器化合物对化工生产有重要意义.
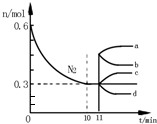
工业合成氨的原理为N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.如图表示在2L的恒容密闭容器中反应时N2的物质的量随时间的变化.
(1)图中0~10min内,用H2表示该反应的平均反应速率为0.045•L-1•min-1,从11min其其他条件不变,压缩容器的体积至1L,则n(N2)的变化曲线为d(填字母);
(2)下表为不同温度下(其他条件相同)该反应的平衡常数,由此可推知,三种温度下,反应从开始至达到平衡时所需时间最长的是T1(填“T1”“T2”或“T3”)
(3)假设在温度为T1℃时,向该密闭容器中同时加入H2,N2,NH3,使c(H2)=0.1mol•L-1,c(N2)=x mol•L-1,c(NH3)=0.1mol•L-1,若要使平衡建立过程中NH3的浓度逐渐减小,则x的取值范围是0≤x<1.
 研究氮机器化合物对化工生产有重要意义.
研究氮机器化合物对化工生产有重要意义.工业合成氨的原理为N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1.如图表示在2L的恒容密闭容器中反应时N2的物质的量随时间的变化.
(1)图中0~10min内,用H2表示该反应的平均反应速率为0.045•L-1•min-1,从11min其其他条件不变,压缩容器的体积至1L,则n(N2)的变化曲线为d(填字母);
(2)下表为不同温度下(其他条件相同)该反应的平衡常数,由此可推知,三种温度下,反应从开始至达到平衡时所需时间最长的是T1(填“T1”“T2”或“T3”)
| T/℃ | T1 | T2 | T3 |
| K | 10 | 2.5 | 1.8 |
1.每年的6月26日是国际禁毒日.如图所示是四种毒品的结构简式,下列有关说法正确的是( )

| A. | 四种毒品中都含有苯环,都属于芳香烃 | |
| B. | 摇头丸经消去、加成反应可制得冰毒 | |
| C. | 1mol大麻与溴水反应最多消耗4mol Br2 | |
| D. | 氯胺酮分子中环上所有碳原子可能共平面 |
18.某饱和一元醇C7H15OH发生消去反应,只得到两种单烯烃,则该醇的结构简式可能是下列( )
| A. | 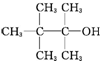 | B. | CH3(CH2)5CH2OH | C. |  | D. | 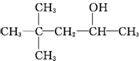 |
5.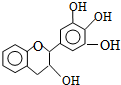 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
 “茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )
“茶倍健”牙膏中含有茶多酚,但茶多酚是目前尚不能人工合成的纯天然、多功能、高效能的抗氧化剂和自由基净化剂.其中没食子儿茶素(EGC)的结构如图所示.关于EGC的下列叙述中正确的是( )| A. | 分子式为C15H12O5 | |
| B. | 分子中所有的原子共面 | |
| C. | 1molEGC与4molNaOH恰好完全反应 | |
| D. | 易发生氧化反应和取代反应,难发生加成反应 |
2.下列有机物在核磁共振氢谱上只有一组峰的是( )
| A. | HCHO | B. | CH3OH | C. | HCOOH | D. | CH3COOCH3 |
19.可逆反应:在密闭容器反应2NO2?2NO+O2,达到平衡状态的标志是( )
(1)单位时间内生成2moL NO2的同时生成2moL NO
(2)单位时间内生成2moL NO的同时,生成1moL O2
(3)用反应物和生成物的物质的量浓度变化表示反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的平均相对分子质量不再改变的状态.
(1)单位时间内生成2moL NO2的同时生成2moL NO
(2)单位时间内生成2moL NO的同时,生成1moL O2
(3)用反应物和生成物的物质的量浓度变化表示反应速率的比为2:2:1的状态
(4)混合气体的颜色不再改变的状态
(5)混合气体的平均相对分子质量不再改变的状态.
| A. | (1)(4)(5) | B. | (2)(3)(5) | C. | (1)(3)(4) | D. | (1)(2)(3)(4)(5) |