题目内容
7.下列叙述及评价均合理的是( )| 选项 | 叙述 | 评价 |
| A | 乙酸乙酯在H218 O中水解,产物乙醇中将含有18O | 错,根据酯的水解规律,产物乙酸中将含有18O同位素,而乙醇则没有. |
| B | 淀粉与20%的硫酸混合溶液在沸水浴中充分加热后滴加碘水无蓝色现象,则说明淀粉水解完全 | 错,淀粉水解后未加碱中和至溶液呈碱性. |
| C | 向卤代烃水解后的溶液中加入AgNO3溶液,根据沉淀颜色可以判断卤素原子种类 | 对,水解后溶液中有卤化氢,与AgNO3溶液反应生成卤化银沉淀. |
| D | 可以用新制的Cu(OH)2悬浊液鉴别乙醇溶液、乙酸溶液和葡萄糖溶液 | 错,用新制的Cu(OH)2悬浊液不能鉴别乙醇溶液和乙酸溶液. |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙酸和乙醇发生酯化反应时“酸脱羟基醇脱氢”,乙酸乙酯的水解为酯化反应的逆反应;
B.检验淀粉不需要加碱中和;
C.水解后,检验卤素离子应在酸性溶液中;
D.新制的Cu(OH)2悬浊液分别与乙酸、乙醇和葡萄糖混合的现象为:蓝色溶液、无现象、砖红色沉淀.
解答 解:A.乙酸乙酯在H218O中水解生成CH3CO18OH和C2H5OH,因此评价正确,故A正确;
B.淀粉与20%的硫酸混合溶液,加热到80℃左右,冷却后取少量水解液滴加碘水无蓝色现象,则说明淀粉水解完全,不需要加碱中和,评价错误,故B错误;
C.卤代烃中加入NaOH溶液,水解后,检验卤素离子应在酸性溶液中,则应先加硝酸至酸性,再加入AgNO3溶液检验,故C错误;
D.新制的Cu(OH)2悬浊液分别与乙酸、乙醇和葡萄糖混合的现象为:蓝色溶液、无现象、砖红色沉淀,现象不同,可以鉴别,故D错误;
故选A.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系、有机反应及有机物检验等为解答的关键,综合性较强,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
18.常温下的4种混合溶液,分别由等体积0.1mol/L的2种溶液混合而成
①NH4Cl与NaOH ②NH4Cl与HCl ③NH4Cl与NaCl ④NH4Cl与NaHCO3
下列各项正确的是( )
①NH4Cl与NaOH ②NH4Cl与HCl ③NH4Cl与NaCl ④NH4Cl与NaHCO3
下列各项正确的是( )
| A. | PH大小顺序①>④>③>② | |
| B. | C(NH3•H2O)大小顺序:②>④>③>① | |
| C. | 混合溶液④中存在C(NH3•H2O)+C(CO32-)+C(H+)=C(OH-)+C(H2CO3) | |
| D. | 混合溶液③中水的电离被促进,其中C(H+)和C(OH-)均大于1.0×10-7mol/L |
18.关于硝酸的说法正确的是( )
| A. | 硝酸电离出的H+离子,能被Zn、Fe等金属还原成H2 | |
| B. | 浓HNO3与浓HCl按3:1的体积比所得的混合物叫王水 | |
| C. | 硝酸与金属反应时,主要是+5价的氮元素得电子 | |
| D. | 常温下,向浓HNO3中投入Fe片,会产生大量的红棕色气体 |
15.下列电池工作时,O2在正极放电的是( )
| A. |  锌锰电池 | B. |  氢燃料电池 | ||
| C. |  铅蓄电池 | D. |  镍镉电池 |
2.有下列几种说法:①含同元素的微粒的化学性质不一定相同;②相对分子质量相同的物质如果结构不同则互为同分异构体;③同分异构体的化学性质一定相同;④同系物具有相同的通式;⑤同系物的化学性质相似;⑥互为同系物的物质间不可能互为同分异构体;⑦两相邻同系物的相对分子质量相差14;⑧化学式相同,各元素质量分数也相同的物质一定是同种物质;以上说法中不正确的是( )
| A. | ②③④ | B. | ②③⑧ | C. | ③④⑤⑦⑧ | D. | ②⑥⑦⑧ |
19.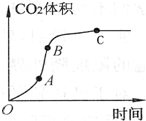 某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积
某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积
的变化),实验结果如图所示,下列说法错误的是( )
 某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积
某学生用优质大理石与稀盐酸反应制取CO2,(不考虑反应过程中溶液体积的变化),实验结果如图所示,下列说法错误的是( )
| A. | AB段反应速率最快的原因可能是反应放热,体系温度升高 | |
| B. | BC段反应速率变慢的原因可能是盐酸浓度降低 | |
| C. | 该反应速率也可以用CaCl2的浓度变化与时间关系来表示 | |
| D. | C点后CO2体积不变的原因一定是盐酸消耗完 |
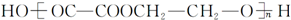 的合成路线如下:[括号内为反应类型,□内为目标产物]
的合成路线如下:[括号内为反应类型,□内为目标产物]
 的化学反应方程式nHOCH2CH2OH+nHOOC-COOH$→_{△}^{浓硫酸}$
的化学反应方程式nHOCH2CH2OH+nHOOC-COOH$→_{△}^{浓硫酸}$ +(2n-1)H2O.
+(2n-1)H2O.