题目内容
【题目】短周期非金属元素B、C、N、O、P、S、Cl,可形成各种单质、化合物的分子。
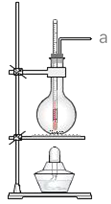
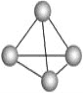
(1)意大利罗马大学的FulvioCacace等人获得了极具理论研究意义的气态N4分子,其分子结构如图。已知断裂1molN—N吸收167kJ热量,生成1molN![]() N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是___。
N放出942kJ热量,根据以上信息和数据,判断下列说法不正确的是___。
A.N4属于一种新型的化合物
B.N4分子中N—N键角为60°
C.N4分子中存在非极性键
D.1molN4转变成N2将吸收882kJ热量
(2)1919年,Langmuir提出等电子体的概念,由短周期元素组成的粒子,只要其原子数相同,各原子的最外层电子数之和相同,也可互称为等电子体。等电子体的结构相似、物理性质相似。与CO互为等电子体的分子和离子分别为___和___(写1种,填化学式)。
(3)BF3和过量NaF作用可生成NaBF4,BF![]() 的空间立体构型为___。
的空间立体构型为___。
【答案】AD N2 CN-(或C![]() 、NO+) 正四面体
、NO+) 正四面体
【解析】
(1)A.N4由一种元素组成,是单质,故A错误;
B.N4分子是正四面体结构N—N键角为60°,故B正确;
C.N4分子中成键的原子相同,存在非极性键,故C正确;
D.N4=2N2,1molN4气体中含有6molN-N键,可生成2molN2,形成2molN≡N键,则1molN4气体转变为N2化学键断裂断裂吸收的热量为:6×167kJ=1002kJ,形成化学键放出的热量为1884kJ,所以反应放热,放出的热量为:1884kJ-1002kJ=882kJ,故应为放出882kJ热量,故D错误;
故答案为:AD;
(2)根据价电子迁移法和电子-电荷互换法得与CO互为等电子体的分子和离子分别为N2和CN-(或C![]() 、NO+),故答案为:N2;CN-(或C
、NO+),故答案为:N2;CN-(或C![]() 、NO+);
、NO+);
(3)BF![]() 的中心原子B为sp3杂化,空间立体构型为正四面体。故答案为:正四面体。
的中心原子B为sp3杂化,空间立体构型为正四面体。故答案为:正四面体。

 名校课堂系列答案
名校课堂系列答案【题目】已知:CH3CH2CH2CH2OH→CH3CH2CH2CHO
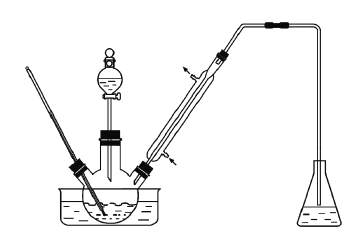
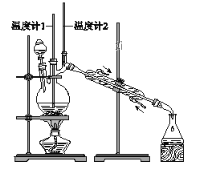
利用下图装置用正丁醇合成正丁醛。相关数据如下:
物质 | 沸点/℃ | 密度/(g·cm-3) | 水中溶解性 |
正丁醇 | 117.2 | 0.8109 | 微溶 |
正丁醛 | 75.7 | 0.8017 | 微溶 |
下列说法中,不正确的是( )
A. 为防止产物进一步氧化,应将酸化的Na2Cr2O7溶液逐滴加入正丁醇中
B. 向获得的粗正丁醛中加入少量金属钠,检验其中是否含有正丁醇
C. 反应结束,将馏出物倒入分液漏斗中,分去水层,粗正丁醛从分液漏斗上口倒出
D. 当温度计1示数为90~95℃,温度计2示数在76℃左右时,收集产物