题目内容
【题目】离子方程式![]() 中的
中的![]() 不能代表的物质是
不能代表的物质是![]()
①![]() ②
②![]() ③
③![]() ④
④![]() ⑤
⑤![]()
A.①③B.①④⑤C.②④⑤D.②⑤
【答案】C
【解析】
依据离子方程式![]() 中的
中的![]() 是溶于水的强酸溶液中发生的反应,同时不能和钡离子反应生成沉淀分析。
是溶于水的强酸溶液中发生的反应,同时不能和钡离子反应生成沉淀分析。
①![]() 溶于水完全电离,且不和钡离子反应,可以代表碳酸钡和盐酸反应的离子方程式,故①不选;
溶于水完全电离,且不和钡离子反应,可以代表碳酸钡和盐酸反应的离子方程式,故①不选;
②![]() 于水完全电离,但硫酸根离子和钡离子结合会生成硫酸钡沉淀,离子方程式为
于水完全电离,但硫酸根离子和钡离子结合会生成硫酸钡沉淀,离子方程式为![]() 不可以代表碳酸钡和硫酸反应的离子方程式,故②选;
不可以代表碳酸钡和硫酸反应的离子方程式,故②选;
③![]() 溶于水完全电离,不和钡离子反应可以代表;可以代表碳酸钡和硝酸反应的离子方程式,故③不选;
溶于水完全电离,不和钡离子反应可以代表;可以代表碳酸钡和硝酸反应的离子方程式,故③不选;
④![]() 中的硫酸根离子和钡离子结合生成沉淀硫酸钡,离子方程式为
中的硫酸根离子和钡离子结合生成沉淀硫酸钡,离子方程式为![]() 不可以代表碳酸钡和硫酸氢钠反应的离子方程式,故④选;
不可以代表碳酸钡和硫酸氢钠反应的离子方程式,故④选;
⑤![]() 是弱酸存在电离平衡,不能写成氢离子的形式,离子方程式
是弱酸存在电离平衡,不能写成氢离子的形式,离子方程式![]() 不可以代表碳酸钡和乙酸反应的离子方程式,故⑤选;
不可以代表碳酸钡和乙酸反应的离子方程式,故⑤选;
故答案选C。

【题目】Ⅰ.查阅资料,乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸。
(1)已知高锰酸钾能氧化草酸.反应如下(部分产物和生成物未写):MnO![]() +H2C2O4→Mn2++CO2↑。若把该反应设计成一原电池,则正极的电极反应式为___。
+H2C2O4→Mn2++CO2↑。若把该反应设计成一原电池,则正极的电极反应式为___。
(2)某同学将2.52g草酸晶体(H2C2O42H2O)加入到100mL0.2molL-1的NaOH溶液中充分反应,测得反应后溶液呈酸性,则其中含碳元素的粒子中物质的量浓度最小的微粒化学式为___。
Ⅱ.某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,发现反应速率变化如图所示,小组成员探究t1~t2时间内速率变快的主要原因,为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种。
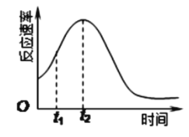
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
(3)猜想Ⅱ可能是:___。
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容。
试管A | 试管B | |
加入试剂 | 2mL0.1mol/LH2C2O4溶液、1mL0.05mol/L酸性KMnO4 | 2mL0.1mol/LH2C2O4溶液、1mL0.05mol/L酸性KMnO4,少量___固体(填物质名称) |
实验现象 (褪色时间) | 褪色时间10min | 褪色时间___10min (选填“<”“>”或“=”) |
结论 | 猜想Ⅱ正确 | |
Ⅲ.为了测定含有H2C2O4·2H2O、KHC2O4和K2SO4的试样中各物质的质量分数,进行如下实验:
①称取6.0g试样,加水溶解,配成250mL试样溶液。
②用酸式滴定管量取25.00mL试样溶液放入锥形瓶中,并加入2~3滴酚酞试液,用0.2500mol/LNaOH溶液滴定,消耗NaOH溶液20.00mL。
③再取25.00mL试样溶液放入另一锥形瓶中,用0.1000mol/L的酸性高锰酸钾溶液滴定,消耗高锰酸钾溶液16.00mL。
回答下列问题:
(5)步骤③中判断滴定终点的方法是___。
(6)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,则测得H2C2O4·2H2O的质量分数___。(填“偏大”、“偏小”或“无影响”)