题目内容
【题目】在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物![]() 如图所示
如图所示![]() ,发生反应:
,发生反应:![]() 保持温度不变,测得平衡时的有关数据如下:
保持温度不变,测得平衡时的有关数据如下:
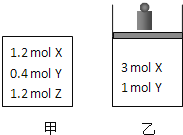
恒容容器甲 | 恒压容器乙 | |
Y的物质的量 |
|
|
Z的体积分数 |
|
|
下列说法正确的是![]()
A.平衡时容器乙的容积一定比反应前小
B.![]()
C.![]()
D.平衡时容器甲的压强一定比反应前大
【答案】A
【解析】
A.容器乙内反应向正反应方向进行,气体总的物质的量减少,恒温恒压下,体积之比等于物质的量之比,所以平衡时容器乙的容积一定比反应前小,故A正确;
B.容器甲内反应所达到的平衡状态可以等效为开始投入3molX,1molY在相同条件下达到的平衡状态,容器乙开始投入虽然也是3molX,1molY,但是保持恒压,反应前后气体分子数减小,则容器乙中反应正向进行的程度较甲中大,则![]() ,故B错误;
,故B错误;
C.同B项分析,容器乙所到达的平衡状态可以等效为容器甲增加压强,平衡向体积减小方向移动,即向正反应方向移动,所以![]() ,故C错误;
,故C错误;
D.容器甲内反应根据有关数据无法判断反应向哪个方向进行、还是处于平衡状态,因此无法判断平衡时容器内的压强与反应前压强大小关系,故D错误。
故选A。

 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案【题目】下表是元素周期表的一部分, 针对表中的①~⑩种元素,填写下列空白:
主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
2 | ① | ② | ③ | |||||
3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
4 | ⑨ | ⑩ |
(1)元素⑩名称为_______在周期表中的位置________________。
(2)在最高价氧化物的水化物中,酸性最强的化合物的分子式是_______,碱性最强的化合物的电子式是:_____________。
(3)元素④与⑥形成的化合物的电子式为:
(4)写出一种由上述元素组成的既有离子键又有非极性共价键的物质的化学式________。
(5)⑥、⑦、⑨三种元素形成的离子,离子半径由大到小的顺序是___________________(用离子符号表示)。
