题目内容
【题目】反应A+3B=2C+D在四种不同情况下的反应速率分别为:
①v(A) =0.15mol/(L·s) ②v(B)=0.6mol/(L·s) ③v(C)=0.5mol/(L·s) ④v (D) =0.45mol/(L·s),则反应进行由快到慢的顺序为:
A.④>③>①>②B.②>④>③>①
C.②>③>④>①D.④>③>②>①
【答案】A
【解析】
同一化学反应方程式中,不同物质表示该反应的反应速率数值可能不同,但表示的意义完全相同,都是表示该反应的反应速率。并且,在同一化学反应方程式中,不同物质的速率之比等于化学计量数之比,所以,比较同一反应的反应速率快慢,需要将反应速率转化为同一种物质的反应速率才能比较;假设均将反应速率转化为v(B)的反应,则①v(A)=3v(B)=0.15mol/(L·s),得v(B)=0.05mol/(L·s);②v(B)=0.6mol/(L·min) =0.01mol/(L·s);③v(C)=![]() v(B)=0.5mol/(L·s),得v(B)=0.75mol/(L·s);④v(D)=
v(B)=0.5mol/(L·s),得v(B)=0.75mol/(L·s);④v(D)=![]() v(B)=0.45mol/(L·s),得v(B)=1.35mol/(L·s);所以,正确的关系为:④>③>①>②;
v(B)=0.45mol/(L·s),得v(B)=1.35mol/(L·s);所以,正确的关系为:④>③>①>②;
答案选A。

练习册系列答案
相关题目
【题目】在温度、初始容积相同的两个密闭容器中,按不同方式投入反应物![]() 如图所示
如图所示![]() ,发生反应:
,发生反应:![]() 保持温度不变,测得平衡时的有关数据如下:
保持温度不变,测得平衡时的有关数据如下:
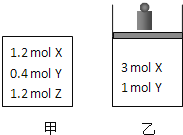
恒容容器甲 | 恒压容器乙 | |
Y的物质的量 |
|
|
Z的体积分数 |
|
|
下列说法正确的是![]()
A.平衡时容器乙的容积一定比反应前小
B.![]()
C.![]()
D.平衡时容器甲的压强一定比反应前大