题目内容
【题目】汽车尾气中的NO与CO发生如下反应2NO(g)+2CO(g) ![]() N2(g)+2CO2(g) ΔH<0,下列说法中错误的是
N2(g)+2CO2(g) ΔH<0,下列说法中错误的是
A. 该反应中反应物的总能量高于生成物的总能量
B. 升高温度,正反应速率加快,逆反应速率减慢
C. 升高温度,NO转化率减小
D. 使用合适的催化剂,能增大反应速率
【答案】B
【解析】
A、放热反应中反应物的总能量高于生成物的总能量;
B、升高温度,正、逆反应的速率都增大;
C、升高温度,平衡向吸热反应方向移动;
D、使用催化剂,降低反应活化能,可以加快反应速率。
A项、该反应为放热反应,放热反应中反应物的总能量高于生成物的总能量,故A正确;
B项、升高温度,正、逆反应的速率都增大,故B错误;
C项、该反应为放热反应,升高温度,平衡向为吸热反应的逆反应方向移动,NO转化率减小,故C正确;
D项、使用催化剂,降低反应活化能,可以加快反应速率,故D正确。

【题目】焦炭是重要的工业原材料。
(1)已知在一定温度下,C(s)+CO2(g) ![]() 2CO(g) 平衡常数K1;C(s)+H2O(g)
2CO(g) 平衡常数K1;C(s)+H2O(g) ![]() CO(g)+H2(g) 平衡常数K2 ;CO(g)+H2O(g)
CO(g)+H2(g) 平衡常数K2 ;CO(g)+H2O(g) ![]() H2(g)+CO2(g) 平衡常数K。则K、K1、K2,之间的关系是__________。
H2(g)+CO2(g) 平衡常数K。则K、K1、K2,之间的关系是__________。
(2)用焦炭还原NO的反应为:2NO(g)+ C(s)![]() N2(g) + CO2(g) ΔH,向容积均为1L的甲、乙、丙三个恒温(反应温度分别为400℃、T ℃、400℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g) + CO2(g) ΔH,向容积均为1L的甲、乙、丙三个恒温(反应温度分别为400℃、T ℃、400℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(NO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
n(NO)(丙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
①甲容器中,0~40 min内用NO的浓度变化表示的平均反应速率v(NO)=_____________ ;
②该反应的平衡常数表达式为__________________;400℃,该反应的平衡常数为_______;
③乙容器的反应温度T____400 ℃(填“>”“<”或“=”)
④丙容器达到平衡时,NO的转化率为___________;平衡时CO2的浓度为________。
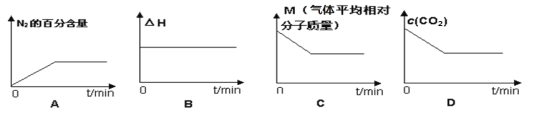
⑤在恒容密闭容器中加入焦炭并充入NO气体,下列图像正确且能说明反应达到平衡状态的是___。