题目内容
若(NH4)2SO4加强热分解的产物是SO2、N2、NH3和H2O,则对该反应的下列说法中正确的是( )
| A.化学方程式中产物分子的化学计量数由小到大的顺序是SO2、N2、NH3、H2O |
| B.氧化产物和还原产物的物质的量之比为3∶1 |
| C.被氧化元素原子和被还原元素原子的物质的量之比为2∶3 |
| D.若反应生成1 mol H2O,则转移的电子为6 mol |
C
解析

练习册系列答案
 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案
相关题目
标准状况下,将a L SO2和Cl2组成的混合气体通入100 mL 0.2 mol·L-1Fe2(SO4)3溶液中,充分反应后,溶液的棕黄色变浅。向反应后的溶液中加入足量的BaCl2溶液,将所得沉淀过滤、洗涤、干燥后称重,其质量为23.3 g。则下列关于该过程的推断不正确的是
| A.混合气体中氯气物质的量为0.04 mol |
| B.混合气体中SO2物质的量为0.04 mol |
| C.所得的沉淀为0.1 mol BaSO4 |
| D.a的取值范围为1.344< a <1.792 |
已知反应:O3 + 2I- + H2O = O2 + I2 + 2OH-,下列说法不正确的是
| A.O3和O2是同素异形体 | B.H2O既不是氧化剂也不是还原剂 |
| C.氧化性:I2>O2 | D.反应生成1mol I2时转移2 mol电子 |
LiAlH4是重要的储氢材料,其组成类似于Na3AlF6。常见的供氢原理如下面两个方程式所示:
①2LiAlH4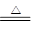 2LiH+2Al+3H2↑
2LiH+2Al+3H2↑
②LiAlH4+2H2O=LiAlO2+4H2↑
下列说法正确的是( )
| A.LiAlH4是共价化合物,LiH是离子化合物 |
| B.生成等质量的氢气,反应①、②转移电子数之比为4?3 |
| C.氢化锂也是一种储氢材料,供氢原理为LiH+H2O=LiOH+H2↑ |
| D.若反应①中生成3.36 L氢气,则一定有2.7 g铝生成 |
某容器中发生一个化学反应,反应过程中存在H2O、ClO-、CN-、HCO3—、N2、Cl-六种物质。在反应过程中测得ClO-和N2的物质的量随时间变化的曲线如图所示。下列有关判断中正确的是( )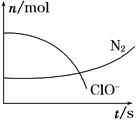
| A.还原剂是含CN-的物质,氧化产物只有N2 |
| B.氧化剂是ClO- , 还原产物是HCO3— |
| C.配平后氧化剂与还原剂的化学计量数之比为5∶2 |
| D.若生成2.24 L N2(标准状况),则转移电子0.5 mol |
LiNiO2是锂离子电池的正极活性材料,其制备原理可表示为4Ni(OH)2+4LiOH+O2=4LiNiO2+6H2O。下列说法正确的是( )
| A.LiNiO2中Ni的化合价是+1 | B.该反应中LiOH是还原剂 |
| C.OH-和Li+含有的电子数相同 | D.LiNiO2中既含离子键又含共价键 |
工业上可用硫酸铝与硫黄焙烧制备氧化铝:2Al2(SO4)3+3S  2Al2O3+9SO2↑,下列有关说法中正确的是( )
2Al2O3+9SO2↑,下列有关说法中正确的是( )
| A.反应中Al2(SO4)3被氧化 |
| B.Al2(SO4)3、Al2O3均含有离子键和共价键 |
| C.5.1 g Al2O3含有9.03×1022个阴离子 |
| D.该反应中,每转移0.3 mol电子生成5.04 L SO2 |
某化学兴趣小组在奥运五连环中填入了5种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型和属于氧化还原反应的个数有( )
| A.复分解反应、1个 | B.分解反应、2个 |
| C.化合反应、3个 | D.置换反应、2个 |