题目内容
7.一定条件下密闭容器中发生如下反应:N2(g)+3H2(g)$\frac{\underline{\;\;催化剂\;\;}}{高温高压}$2NH3(g),能说明该反应达到化学平衡状态的是( )| A. | 生成NH3的物质的量与消耗NH3的物质的量相等 | |
| B. | 消耗1molN2,同时消耗3molH2 | |
| C. | N2、H2、NH3在密闭容器中共存 | |
| D. | 正、逆反应速率都等于0 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、生成NH3的物质的量与消耗NH3的物质的量相等,正逆反应速率相等,达平衡状态,故A正确;
B、都反映的是正向,未体现正与逆的关系,不能说明达平衡状态,故B错误;
C、只要反应发生,就是反应物和生成共存的体系,故C错误;
D、化学平衡是动态平衡,当反应达到平衡状态时,正逆反应速率相等,但不为0,故D错误;
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.已知甲酸分子中4个原子共平面.下列分子中所有原子不可能同时存在于同一平面的是( )
| A. | CH2=CH-CH=CH2 | B. | 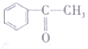 | C. | ClCH=CHCHO | D. | 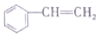 |
18.有四种物质:①NaHCO3、②Al(OH)3、③(NH4)2CO3、④NH2-CH2-COOH,其中既能跟盐酸,又能跟NaOH溶液反应的有( )
| A. | 只有②④ | B. | 只有①② | C. | 只有①②③ | D. | ①②③④ |
2.一定条件下,发生如下反应:2A(g)+2B(g)?3C(g)+D(g)在容积不变的密闭容器中进行,达到化学平衡状态的标志是( )
| A. | 单位时间内生成n mol B,同时消耗3n mol C | |
| B. | 容器内压强不随时间而变化 | |
| C. | 混合气体的密度不随时间变化 | |
| D. | 单位时间内生成2n mol A,同时生成n mol D |
19.当CH3COOH?CH3COO-+H+已达平衡,若要使醋酸的电离平衡向左移动和溶液的pH值都减小,应加入的试剂是( )
| A. | CH3COONa | B. | NH3•H2O | C. | HCl | D. | H2O |
16.某链状有机物分子中含m个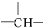 ,n个-C2H5,a个
,n个-C2H5,a个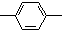 ,其余为氯原子,则氯原子的数目可能是( )
,其余为氯原子,则氯原子的数目可能是( )
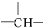 ,n个-C2H5,a个
,n个-C2H5,a个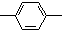 ,其余为氯原子,则氯原子的数目可能是( )
,其余为氯原子,则氯原子的数目可能是( )| A. | m+2-n | B. | n+2a-3m | C. | n+m+a | D. | a+n+2-2m |
17.物质的量浓度相同(0.1mol•L-1)的弱酸HX与NaX溶液等体积混合后,溶液中粒子浓度关系错误的是( )
| A. | c(Na+)+c(H+)=c(X-)+c(OH-) | |
| B. | 若混合液呈酸性,则c(X-)>c(Na+)>c(HX)>c(H+)>c(OH-) | |
| C. | c(HX)+c(X-)=2c(Na+) | |
| D. | 若混合液呈碱性,则c(Na+)>c(HX)>c(X-)>c(OH-)>c(H+) |
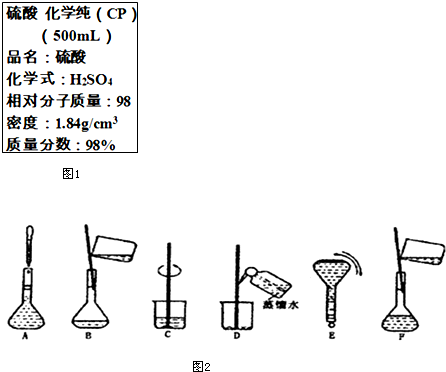 如图1是硫酸试剂瓶标签上的部分内容.现实验室需要240ml 4.6mol/L的稀硫酸用该硫酸配置,
如图1是硫酸试剂瓶标签上的部分内容.现实验室需要240ml 4.6mol/L的稀硫酸用该硫酸配置, Na2S
Na2S
 CO2
CO2 .
.