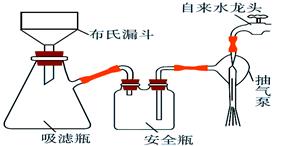
题目内容
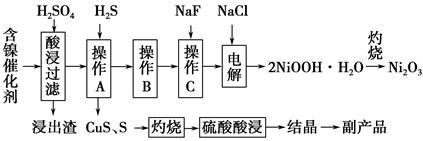
氧化镁在医药、建筑等行业应用广泛。硫酸镁还原热解制备高纯氧化镁是一种新的探索。以菱镁矿(主要成分为MgCO3,含少量FeCO3 )为原料制备高纯氧化镁的实验流程如下:
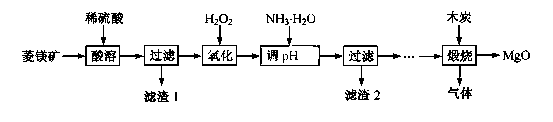
生成氢氧化物沉淀的pH
(1)MgCO3与稀硫酸反应的离子方程式为 。
(2)加氨水调节溶液的PH范围为 。
(3)滤渣2 的成分是 (填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C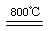 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑
MgSO4+C MgO+SO2↑+CO↑
MgO+SO2↑+CO↑
MgSO4+3C MgO+S↓+3CO↑
MgO+S↓+3CO↑
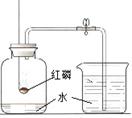
利用下图装置对煅烧产生的气体进行分步吸收或收集。
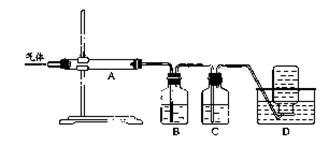
①D中收集的气体是 (填化学式)。
②B中盛放的溶液是 (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硫酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: 。

生成氢氧化物沉淀的pH
| | Mg(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀时 | 9.4 | 6.3 | 1.5 |
| 完全沉淀时 | 12.4 | 8.3 | 2.8 |
(1)MgCO3与稀硫酸反应的离子方程式为 。
(2)加氨水调节溶液的PH范围为 。
(3)滤渣2 的成分是 (填化学式)。
(4)煅烧过程存在以下反应:
2MgSO4+C
 2MgO+2SO2↑+CO2↑
2MgO+2SO2↑+CO2↑MgSO4+C
 MgO+SO2↑+CO↑
MgO+SO2↑+CO↑ MgSO4+3C
 MgO+S↓+3CO↑
MgO+S↓+3CO↑利用下图装置对煅烧产生的气体进行分步吸收或收集。

①D中收集的气体是 (填化学式)。
②B中盛放的溶液是 (填字母)。
a.NaOH 溶液 b.Na2CO3溶液 c.稀硫酸 d.KMnO4溶液
③A中得到的淡黄色固体与热的NaOH溶液反应,产物中元素最高价态为+4,写出该反应的离子方程式: 。
(1)MgCO3+2H+=Mg2++CO2↑+H2O
(2)2.8<PH<9.4
(3)Fe(OH)3
(4)①CO ②d ③3S+6OH- 2S2-+SO32-+3H2O(3分)
2S2-+SO32-+3H2O(3分)
(2)2.8<PH<9.4
(3)Fe(OH)3
(4)①CO ②d ③3S+6OH-
 2S2-+SO32-+3H2O(3分)
2S2-+SO32-+3H2O(3分)试题分析:(1)MgCO3是难溶电解质,书写离子方程式时不能拆开,所以MgCO3与稀硫酸反应的离子方程式为MgCO3+2H+=Mg2++CO2↑+H2O
(2)加氨水调节溶液的PH的目的是使铁元素沉淀而镁不能沉淀,铁元素在溶液中以铁离子存在,所以溶液的PH的范围是2.8<PH<9.4
(3)铁元素在溶液中以铁离子存在,所以滤渣2的成分是Fe(OH)3
(4)①右图装置对煅烧产生的气体进行分步吸收或收集,所以最终的剩余气体为CO,②短少的气体产物有SO2、CO2、CO,三种气体分步被吸收或收集,SO2、CO2都能与a、b反应,与c都不能反应,而高锰酸钾溶液可与SO2反应,所以B中应放高锰酸钾溶液吸收SO2,答案选d。③淡黄色固体为S,与热的NaOH溶液发生歧化反应,S被氧化为SO32-,同时被还原成S2-,其离子方程式为3S+6OH-
 2S2-+SO32-+3H2O
2S2-+SO32-+3H2O
练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目