题目内容
氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域.在一定条件下,氮化铝可通过如下反应合成:Al2O3+N2+3C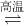 2AlN+3CO下列有关该反应的叙述不正确的是
2AlN+3CO下列有关该反应的叙述不正确的是
- A.氮化铝中氮元素的化合价为-3
- B.上述反应中每生成2molAlN,N2得到6mol电子
- C.在氮化铝的合成反应中,N2是氧化剂,Al2O3是还原剂
- D.该反应不属于四种基本反应类型中任意一种
C
分析:Al2O3+N2+3C 2AlN+3CO中,碳元素的化合价由0升高到+2价,氮元素的化合价由0降低为-3价,反应中共转移6mol电子,以此来解答.
2AlN+3CO中,碳元素的化合价由0升高到+2价,氮元素的化合价由0降低为-3价,反应中共转移6mol电子,以此来解答.
解答:A、AlN中Al为+3价,因化合价中正负化合价的代数和为0,则N元素的化合价为-3价,故A正确;
B、因氮元素的化合价由0降低为-3价,则每生成2molAlN,N2得到2mol×(3-0)=6mol电子,故B正确;
C、在氮化铝的合成反应中,N2是氧化剂,C是还原剂,故C错误;
D、该反应是氧化还原反应,生成物都是化合物,反应物有三种,则不属于四种基本反应类型中任意一种,故D正确;
故选C.
点评:本题考查氧化还原反应,明确该反应中N、C元素的化合价变化是解答本题的关键,并利用化合价来分析电子的转移、利用四种反应物与生成物来分析与四种基本反应类型的关系.
分析:Al2O3+N2+3C
 2AlN+3CO中,碳元素的化合价由0升高到+2价,氮元素的化合价由0降低为-3价,反应中共转移6mol电子,以此来解答.
2AlN+3CO中,碳元素的化合价由0升高到+2价,氮元素的化合价由0降低为-3价,反应中共转移6mol电子,以此来解答.解答:A、AlN中Al为+3价,因化合价中正负化合价的代数和为0,则N元素的化合价为-3价,故A正确;
B、因氮元素的化合价由0降低为-3价,则每生成2molAlN,N2得到2mol×(3-0)=6mol电子,故B正确;
C、在氮化铝的合成反应中,N2是氧化剂,C是还原剂,故C错误;
D、该反应是氧化还原反应,生成物都是化合物,反应物有三种,则不属于四种基本反应类型中任意一种,故D正确;
故选C.
点评:本题考查氧化还原反应,明确该反应中N、C元素的化合价变化是解答本题的关键,并利用化合价来分析电子的转移、利用四种反应物与生成物来分析与四种基本反应类型的关系.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
