题目内容
【题目】按要求完成下列各题。
(1)向澄清石灰水中通入过量CO2(写出离子方程式)___________________________________
(2)用稀硫酸洗铁锈(Fe2O3)(写出离子方程式)____________________________________
(3)2Al + 6H+ = 2Al3+ + 3H2↑(写出对应的化学方程式并用双线桥法标出电子转移情况)__________________
(4)在一定条件下,某化合物W受热分解:2W ![]() A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是 _______
A↑+2B↑+4C↑,测得反应后生成的混合气体的密度是相同条件下H2密度的12倍,则W的摩尔质量是 _______
【答案】 CO2+OH-=HCO3- Fe2O3 +6H + =2Fe3+ + 3H2O 略 84g/mol
【解析】(1)向澄清石灰水中通入过量CO2反应生成碳酸氢钙和水,该离子反应为: CO2+OH-=HCO3-因此,本题正确答案为: CO2+OH-=HCO3-
(2)用稀硫酸洗铁锈( Fe2O3 )反应生成硫酸铁和水,该离子反应为:Fe2O3 +6H + =2Fe3+ + 3H2O
因此,本题正确答案为:Fe2O3 +6H + =2Fe3+ + 3H2O
(3)Al与盐酸的离子反应为2Al + 6H+ = 2Al3+ + 3H2↑,该反应为![]() ,该反应中Al元素由0价升高为+3价,H元素由+1价降低为0价,双线桥法标出电子转移为
,该反应中Al元素由0价升高为+3价,H元素由+1价降低为0价,双线桥法标出电子转移为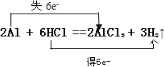 ,因此,本题正确答案为:
,因此,本题正确答案为: .
.
(3)令W的物质的量为![]() ,由方程式2W
,由方程式2W ![]() A↑+2B↑+4C↑,可以知道混合气体总物质的量为
A↑+2B↑+4C↑,可以知道混合气体总物质的量为![]() ,混合气体对氢气的相对密度为12,则混合气体平均摩尔质量=12
,混合气体对氢气的相对密度为12,则混合气体平均摩尔质量=12![]() 2g/mol=24g/mol,混合气体总质量=7mol
2g/mol=24g/mol,混合气体总质量=7mol![]() 24g/mol=168g,由质量守恒定律可以知道W的质量等于混合气体总质量,故W的摩尔质量=
24g/mol=168g,由质量守恒定律可以知道W的质量等于混合气体总质量,故W的摩尔质量=![]() =84g/mol。因此,本题正确答案为:84g/mol
=84g/mol。因此,本题正确答案为:84g/mol