题目内容
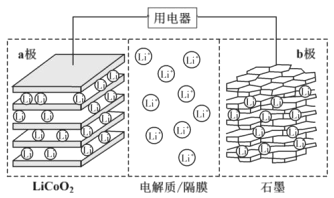
【题目】某兴趣小组设计如下微型实验装置。实验时,先断开K2,闭合K1,两极均有气泡产生;一段时间后,断开K1,闭合K2,发现电流计A指针偏转。下列有关描述正确的是
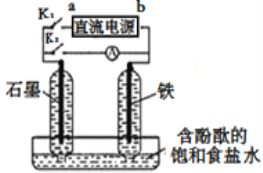
A.断开K2,闭合K1时,总反应的离子方程式为:2Cl-+2H+ ![]() H2↑+Cl2↑
H2↑+Cl2↑
B.断开K2,闭合K1时,a是电源的正极,铁电极发生氧化反应
C.断开K1,闭合K2时,石墨电极附近溶液变红,铁电极上的电极反应为:Cl2+2e—=2Cl-
D.断开K1,闭合K2时,石墨电极作正极
【答案】D
【解析】
A. 断开K2,闭合K1时,是电解池装置,电解饱和食盐水的总反应的离子方程式为2H2O+2Cl-![]() Cl2↑+H2↑+2OH-,故A错误;
Cl2↑+H2↑+2OH-,故A错误;
B. 断开K2,闭合K1时,是电解池装置,两极均有气泡产生,说明两极产生的气体分别是氢气和氯气,因此活泼金属铁不能做阳极,应该是做阴极,则a是电源的正极,铁电极为负极,发生还原反应,故B错误;
C. 断开K1,闭合K2时,发现电流计A指针偏转,证明是原电池反应,形成氢氯燃料电池,断开K2,闭合K1时,铁电极上产生了氢气,石墨电极上产生了氯气,因此铁做负极发生氧化反应,氢气失电子生成氢离子的反应,故C错误;
D. 断开K1,闭合K2时,发现电流计A指针偏转,证明是原电池反应,形成氢氯燃料电池,断开K2,闭合K1时,铁电极上产生了氢气,石墨电极上产生了氯气,因此石墨电极作正极,故D正确;
故选D。

【题目】下列实验操作能达到实验目的或得出相应结论的是
实 验 操 作 | 目的或结论 | |
A | 将Cu片放入FeCl3溶液中 | 证明Fe的金属性比Cu强 |
B | 将点燃的镁条置于盛有CO2的集气瓶中,瓶内壁有黑色固体生成 | 镁与CO2发生置换反应 |
C | 将SO2通入溴水或酸性高锰酸钾溶液中 | 证明SO2有漂白性 |
D | 向FeCl2溶液(含少量FeBr2杂质)中,加入适量氯水,再加CCl4萃取分液 | 除去FeCl2溶液中的FeBr2 |
A. A B. B C. C D. D