��Ŀ����
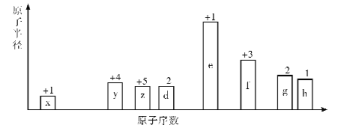
����Ŀ����ѧ��Ӧ�е������仯���ɻ�ѧ��Ӧ�оɻ�ѧ������ʱ���յ��������»�ѧ���γ�ʱ�ų���������ͬ����ġ���ͼΪN2��g����O2��g����Ӧ����NO��g�������е������仯������˵����ȷ����

A.1 mol N2��g����NA�� O2��g����Ӧ�ų�������Ϊ180 kJ
B.1 mol N2��g����1 mol O2��g�������������2 mol NO��g�����������
C.ͨ������£�N2��g����O2��g�������ֱ������NO
D.NO��һ���������������NaOH��Һ��Ӧ�����κ�ˮ
���𰸡�B
��������
A. �ʱ�=��Ӧ�����֮��-���������֮�ͣ���N2(g)+O2(g)=2NO(g) ��H=946kJ/mol+498kJ/mol-2��632kJ/mol=180kJ/mol>0����Ӧ�����ȷ�Ӧ����A����
B. ����A�����֪��Ӧ�����ȷ�Ӧ�����������غ㣬1 mol N2(g)��1 mol O2(g)���е�������С��2 mol NO(g)���е�����������B��ȷ��
C. ͨ������£�N2(g)��O2(g)��ϲ���ֱ������NO����C����
D. NO�Dz����������������NaOH��Һ��Ӧ�����κ�ˮ����D����
��ѡB��

��ϰ��ϵ�д�
�����Ŀ