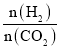题目内容
【题目】某同学对一无色透明溶液进行分析得出该溶液中含有下列某组离子,你认为该组离子应该是
A.Al3+、![]() 、K+、
、K+、![]() B.Ca2+、H+、
B.Ca2+、H+、![]() 、
、![]()
C.OH-、![]() 、
、![]() 、Al3+D.Fe3+、Mg2+、
、Al3+D.Fe3+、Mg2+、![]() 、Clˉ
、Clˉ
【答案】A
【解析】
溶液无色可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子,透明溶液中的离子之间不满足离子反应发生的条件:生成难溶物、生成气体、生成弱电解质、发生氧化还原反应、生成络合物等,在溶液中就能够大量共存。
A.Al3+、NO3-、K+、SO42-之间不发生任何反应,都是无色离子,在溶液中能够大量共存,故A正确;
B.CO32-能够与Ca2+、H+离子发生反应,H+离子能够与AlO2-根离子反应,在溶液中不能大量共存,故B错误;
C.OH-与NH4+、Al3+之间发生反应,在溶液中不能大量共存,故C错误;
D.Fe3+呈现棕黄色,不满足溶液为无色溶液的条件,故D错误;
答案为A。

 阅读快车系列答案
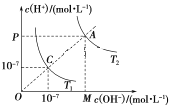
阅读快车系列答案【题目】25 ℃时,0.1 mol·L-1HA溶液中 =108,0.01 mol·L-1BOH溶液pH=12。请回答下列问题:
=108,0.01 mol·L-1BOH溶液pH=12。请回答下列问题:
(1)HA的电离常数Ka为________,BOH是________(填“强电解质”或“弱电解质”)。
(2)pH相等的BOH溶液与BA溶液,分别加热到相同的温度后BOH溶液的pH________(填“>”“=”或“<”)BA溶液的pH。
(3)已知碳酸的Ka1=4.3×10-7,Ka2=5.6×10-11,向等浓度的Na2CO3和NaA的溶液中滴加盐酸直至过量,则与H+作用的粒子依次为___________________。
(4)25 ℃,两种酸的电离平衡常数如下表。
Ka1 | Ka2 | |
H2SO3 | 1.3×10-2 | 6.3×10-8 |
H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO3-的电离平衡常数表达式K=___________________。
②0.10 mol·L-1 NaHSO3溶液中离子浓度由大到小的顺序为_____________________。
③H2SO3溶液和NaHCO3溶液反应的主要离子方程式为______________________。
【题目】已知常温下浓度为0.1mol/L的几种溶液的pH如右下表。下列有关说法正确的是( )
溶质 | pH |
NaF | 7.5 |
Na2CO3 | 11.6 |
NaClO | 9.7 |
NaHCO3 | 8.3 |
A. 同温度同浓度下,酸由强到弱的顺序为:HF>H2CO3>HClO
B. 水解方程式:F-+H2O![]() HF+OH-的平衡常数为1×10-13
HF+OH-的平衡常数为1×10-13
C. 将CO2通入0.lmol/LNa2CO3溶液至溶液呈中性,则溶液中:2c(CO32-)+c(HCO3-)=0.1mol/L
D. 等物质的量的NaF和HF混合溶液中粒子浓度大小关系为:c(HF)>c(Na+)>c(F-)>c (H+)>c(OH-)