题目内容
现有一种碱金属的碳酸盐(M2CO3)和碳酸氢钠组成的混合物,取其1.896g加热至质量不再变化,把放出的气体通入足量的澄清石灰水中,得到白色沉淀0.800g。将加热后残留的固体与足量稀硫酸充分反应,生成的气体经充分干燥后通过足量的过氧化钠粉末,结果过氧化钠粉末增重0.336 g。
(1)试通过计算确定M2CO3的M为何种元素。
(2)有同学提出,通过简单的定性实验,也可以确定该样品中的M为何种碱金属元素。你认为该实验方案是什么?
(1)试通过计算确定M2CO3的M为何种元素。
(2)有同学提出,通过简单的定性实验,也可以确定该样品中的M为何种碱金属元素。你认为该实验方案是什么?
(1)(3分)
2NaHCO3~ Na2CO3 ~ CO2~ CaCO3
n(NaHCO3)=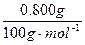 × 2=0.016mol
× 2=0.016mol
2CO2+2Na2O2=2Na2CO3+O2 △m
2mol 56g
(0.012mol) 0.336g
加热后的n(M2CO3)=0.012mol-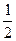 ×0.016mol =0.004mol 设M的相对原子质量分别x。
×0.016mol =0.004mol 设M的相对原子质量分别x。
依题意:84g·mol-1×0.016mol+(2x+60)g·mol-1×0.004mol=1.896g x=39
根据碱金属的相对原子质量,可知M元素是K。
(2)对混合物进行焰色反应实验,透过蓝色的钴玻璃,若看到浅紫色火焰,则说明M元素是K。(2分)
2NaHCO3~ Na2CO3 ~ CO2~ CaCO3
n(NaHCO3)=
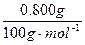 × 2=0.016mol
× 2=0.016mol2CO2+2Na2O2=2Na2CO3+O2 △m
2mol 56g
(0.012mol) 0.336g
加热后的n(M2CO3)=0.012mol-
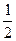 ×0.016mol =0.004mol 设M的相对原子质量分别x。
×0.016mol =0.004mol 设M的相对原子质量分别x。依题意:84g·mol-1×0.016mol+(2x+60)g·mol-1×0.004mol=1.896g x=39
根据碱金属的相对原子质量,可知M元素是K。
(2)对混合物进行焰色反应实验,透过蓝色的钴玻璃,若看到浅紫色火焰,则说明M元素是K。(2分)
略

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 .8 mol HCl,生成0.5mol二氧化碳。求原混合物中NaHCO3的质量分数为多少?
.8 mol HCl,生成0.5mol二氧化碳。求原混合物中NaHCO3的质量分数为多少?