题目内容
3.在298K、100kPa时,已知:2H2O(g)═2H2(g)+O2(g)△H1
Cl2(g)+H2(g)═2HCl(g)△H2
2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3
则△H3与△H2和△H1之间的正确关系是△H3=2△H2+△H1
已知氢气的燃烧热为285.8kJ/mol,则H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8kJ/mol.
分析 根据三个化学反应方程式可知,反应2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)可由另两个反应变形后加和得到,则由盖斯定律可知,△H3应为另两个反应反应热的加和;根据1mol可燃物燃烧生成稳定氧化物放出的热量为燃烧热判断.
解答 解:①2H2O(g)=2H2(g)+O2(g)△H1;
②H2(g)+Cl2(g)=2HCl(g)△H2;
③2Cl2(g)+2H2O(g)=4HCl(g)+O2(g)△H3;
则反应③=2×②+①,
由盖斯定律可知,△H3=2△H2+△H1;
1mol氢气燃烧生成稳定氧化物液态水放出的热量为燃烧热,H2的燃烧热为285.8 kJ/mol,所以H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ/mol,
故答案为:△H3=2△H2+△H1;-285.8 kJ/mol.
点评 本题考查了燃烧热、中和热定义,难度不大,抓住基本概念即可解答.

练习册系列答案
相关题目
11.具有解热镇痛作用的药物是( )
| A. | 阿司匹林 | B. | 青霉素 | C. | NaHCO3 | D. | 麻黄碱 |
18.下列离子方程式书写正确的是( )
| A. | 铁与硫酸铜溶液反应:Fe+Cu2+=Fe2++Cu | |
| B. | 稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ | |
| C. | 碳酸钙与盐酸反应:CO${\;}_{3}^{2-}$+2H+=CO2↑+H2O | |
| D. | 氢氧化钡溶液与稀硫酸反应:Ba2++SO${\;}_{4}^{2-}$=BaSO4↓ |
8.实验室测得4mol SO2发生下列化学反应:2SO2(g)+O2(g)═2SO3(g)△H=-196kJ/mol.当放出313.6kJ热量时,SO2转化率最接近于( )
| A. | 40% | B. | 50% | C. | 80% | D. | 90% |
12.粗盐中含Ca2+、Mg2+、Fe3+、SO42-及泥沙等杂质,需要提纯后才能综合利用.粗盐提纯的步骤有:①加入过量的Na2CO3溶液;②加入过量的BaCl2溶液;③加入过量的NaOH溶液;④加盐酸调节溶液的pH;⑤溶解;⑥过滤; ⑦蒸发.正确的操作顺序是( )
| A. | ⑤①③②④⑥⑦ | B. | ⑤①②③⑥④⑦ | C. | ⑤③①②⑥④⑦ | D. | ⑤③②①⑥④⑦ |
20.已知:①I2+SO2+2H2O═2HI+H2SO4;②2FeCl2+Cl2═2FeCl3;③2FeCl3+2HI═2FeCl2|+2HCl+I2,根据上述反应,判断下列说法正确的是( )
| A. | 氧化性强弱顺序是:Fe3+>Cl2>I2>SO42- | |
| B. | 还原性强弱顺序是:SO2>I->Fe2+>Cl- | |
| C. | 反应Cl2+SO2+2H2O═2HCl+H2SO4不能发生 | |
| D. | Fe3+与I-在溶液可以大量共存 |
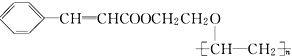

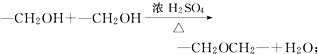
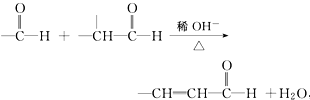
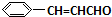 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2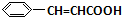 +H2O;
+H2O;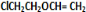 +
+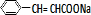 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$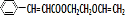 +NaCl.
+NaCl. .
. .
.